当疫苗进入细胞后,它干了什么?
世纪疫情降临人间三年,当COVID-19这个恶魔横扫全球两年后,人类用智慧发明了对抗COVID-19的疫苗。但与此同时,民间也对疫苗提出了很多看法、质疑与顾虑,议论最多的还是疫苗会改变基因这个传言,追溯历史几乎从疫苗出现开始,好长一段时间,就一直伴随着对它的很多质疑和没有医学根据的担忧。 在19世纪,所谓的反疫苗联盟在英国各地纷纷冒起,其中宗教问题是主要的原因。那时候是在1870年代,在英国反疫苗活动人士威廉·泰布(William Tebb)到访过美国后,美国也出现了第一个反疫苗组织。 所以,尽管COVID-19出现,令无数人失去生命。但当疫苗面世的时候,还是有很多人抱着观望的态度,迟迟不敢伸出他的手臂。因为受到坊间传言的影响,在那个时候,我也犹豫过,但很快我就没有任何顾虑了。我的大家庭里面有很多学医的同辈和小辈,那时我一个当医生的同辈发信息来叫我马上去选择莫德纳疫苗,我就毫不犹豫的去打了两针,也算是比较早期的一批。 我自己从小喜欢接触医学知识,尤其对细胞的组织很感兴趣,我总觉得人体的构造是一套很有趣的密码,但如果说到学术方面我的认知还是很肤浅的。

某天我与一位小辈闲聊关于疫苗的话题,她曾是美国Wadsworth Center的研究员. 那是位于纽约州的一所有100年历史的医学科研中心,很大,设备很一流,我去过几次,Wadsworth Center在世界排名很前(几年前好像排第二),她在那里好几年了,与她的导师联合发表过关于细胞的论文,她是专门研究细胞的(主要负责细胞核和粒线体部分)。那天,我就直接问了她本文标题的问题:《当疫苗进入细胞后,它干了什么?》。 开始的时候,她用很专业的词汇给我解析。后来,我希望她用最通俗易懂的方法陈述,因为我也要告诉其他医学常识不高的普通人,让大家弄清楚疫苗与细胞的问题,从而放心地去打疫苗。但她反问我说,你不会也听不懂吧?我说,对于细胞的原理和结构我懂,但疫苗与细胞的关系这个新课题却一知半解。社会上给平民百姓的解析太过教科书了,枯燥难懂,一般人很难理解,所以,就形成很多人因为不了解,所以不理解。 于是,我们就开始尽量普及化、人性化的说开了这个话题:她说,要知道疫苗进入细胞后的工作,就必须要知道人体的结构层次,就是:细胞—分化组织—构成器官—构成系统—组成人体。细胞是生物体结构的基本单位,细胞一般很小,要用光学显微镜才能观察到,但有些又很大,肉眼可见,如鸡蛋、鸭蛋等各种蛋类。(精准一点来说,蛋黄是一颗卵细胞。) 细胞的基本结构有三个主要的地方:细胞膜—用于保护细胞并控制物质的进出。细胞质—作用是介于细胞膜和细胞核之间,是生命活动的场所。细胞核—主要内含遗传物质(即染色体、DNA、基因)。所以我们应该知道的是:一切生物都是由细胞组成的,细胞是生命的基本组成单位,但是一切细胞只能来自原来的细胞的分裂。 细胞具有独立的、有序的自控代谢体系,细胞是代谢与功能的基本单位。所以,细胞是有机体生长与发育的基础。还有最重要的一点,就是细胞是遗传的基本单位,细胞具有遗传的全能性。所以,没有细胞就没有完整的生命。 小小细胞的结构是很复杂的,里面隐藏了12种物质,包括有: 细胞壁、细胞膜、细胞质、细胞核、内质网、核糖体、高基氏体、溶体、液泡、粒线体、叶绿体。 所有细胞都是由水、盐类、核酸、蛋白质、糖、脂质,以及其他各种微量物质如维生素、细胞代谢中间产物等组成的。水、盐离子和某些维生素或与细胞中的大分子组成复合物,或者游离存在。不同细胞或不同的生物中,它们含量的差别往往很大。 细胞周期亦称有丝分裂周期(mitosis cycle),细胞生长到一定程度,不是繁殖就是死亡。细胞分裂后产生的新细胞生长增大,随后又平均地分裂成两个和原来母细胞一样的子细胞,细胞这种生长与分裂的循环称细胞周期。 细胞有机体细胞,依寿命长短不同可划分为两类,即干细胞和功能细胞。干细胞在整个一生都保持分裂能力,直到达到最高分裂次数便衰老死亡。如表皮生发层细胞,生血干细胞等。 细胞是在不断生长繁殖之中,所以存在细胞寿命长短问题,这种长短,各类细胞差别也很大,例如:很多人知道的红细胞寿命大约120天,而神经细胞的数量,出生时有多少以后就有多少,不能增加,可见神经细胞的寿命最长。 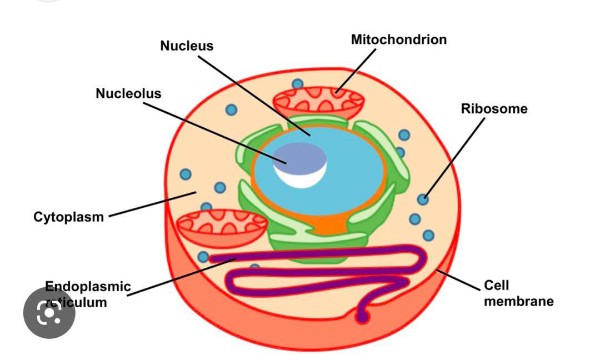
一个细胞的结构有12种类,为了避免本文章篇幅太长,大家看着乏味,所以,我在这里就只简单谈谈比较重要的细胞核、核糖体、粒线体、细胞膜。 1)细胞核(Nucleus) 细胞核是橾控整个细胞的控掣站,主要携带遗传物质(DNA),包括染色体(脱氧核糖核酸加上一些特殊的蛋白质)、核糖核酸等,核膜上有许多小孔称做核孔,由数十种特殊的蛋白组成特别的构造,容许一些物质自由通过,但是分子量很大的核糖核酸、蛋白质就必须依赖这些蛋白辅助,以消耗能量的主动运输,来往于细胞质跟细胞核之间。细胞分裂的期间可以看到细胞核中最显著的构造——核仁,其组成为核糖体RNA,以及合成核糖体所需的蛋白质。除核仁外,细胞核中还有许多其它核细胞器。 有趣的是,有些细胞为了执行特别的工作而没有细胞核:例如:哺乳动物的红血球,为了减少携带的氧气被红血球本身消耗,而成熟后就没有细胞核。 2)核糖体 (Ribosome) 核糖体负责合成蛋白质的胞器,由大、小两个次单元组成,次单元之中有核糖体RNA和核糖体特有的蛋白质,在细胞质中,接受细胞核的遗传讯息、细胞外的刺激讯息,以合成蛋白质,可分为游离核糖体与附着核糖体,前者所制造之蛋白质专用于细胞质内部(不含胞器内部),后者则先经过内质网腔修饰,以小囊泡运输到高基氏体做进一步的分类与修饰,完成的蛋白质主要包装在胞器之中、运到膜上、或是运出细胞之外。 3)粒线体 (Mitochondrion) 粒线体,又称“线粒体”之所以如此称呼,是因为在显微镜下有两类主要的外观,是一种双层膜的胞器,外膜平滑,内膜则朝内部形成皱折状的构造称为折襞,目的是为了增加生理作用的表面积,折襞之间充满基质,其中有许多的代谢反应进行。整个粒线体主要协助细胞呼吸,并且产生细胞使用能量最直接的形式,三磷酸腺苷。特别的是粒线体有自己的遗传分子,与细胞核的遗传物质不同,只遗传到这个胞器的子代胞器,而不是子代细胞,能够让粒线体自我分裂增殖,制造本身需要的一些蛋白质,但是仍有一些调节控制的过程受到细胞核的影响,更重要的是,粒线体基因只在母系遗传(只存在于母体的基因里),它并不遵守孟德尔遗传律。 人体内线粒体最多的细胞是肝脏的肝细胞。每一个肝细胞内约有2000个线粒体。正常线粒体寿命为一周,线粒体可以通过分裂增生。线粒体的主要化学成分为蛋白质,约占65%,其他成分为甘油脂、卵磷脂、脑磷脂和胆固醇等。线粒体内含有多种酶(蛋白质),主要作用是为细胞功能活动不断提供能量,细胞生命活动所必需的总能量中,大约有95%来自线粒体。肝细胞是人体内生命活动最活跃的细胞,所以线粒体对于人的生命非常重要。 4)细胞膜 (Cell membrane) 所有细胞都依赖于极为重要的细胞膜。它的作用就像围栏,在保持细胞内物质的同时允许食物和营养素进入。 细胞膜由磷脂的双层脂肪酸构成。这些脂肪酸分子分为头部和尾部。头部结构称为“亲水结构”,意思是可被水吸引。而尾部结构称为“疏水结构”,意思是可被水排斥。这种头部和尾部的组合造就了细胞膜的结构和功能。 顺便说一下,人体内最大的细胞是卵细胞,最小的细胞是男性的精子,175000个精子细胞才抵得上一个卵细胞的重量。 说到这里,相信大家对人体细胞有了基础的认识了,那么,我们来说说疫苗和疫苗进入细胞的话题吧。 首先,我们都知道现在世界上有4个种类的新冠病毒疫苗。 1)mRNA,2)腺病毒载体,3)重组棘蛋白,4)灭活病毒。 我们再把它们分出两大类,第一类是传统的常规疫苗:(包括了腺病毒载体,重组棘蛋白,灭活病毒。) 另一类就是信使核糖核酸(mRNA)疫苗。 【常规疫苗】 因为每种病毒都各不相同,而COVID-19的病毒被称为SARS-CoV-2。如果没有疫苗,身体就必须要识别病毒、同时学会如何对抗病毒并产生免疫反应。与此同时,病毒在身体里的复制水平和速度会超出身体本身的免疫系统能够处理的水平,这意味着身体会感到不适,继而发病。 那么疫苗是如何制造的呢? 大多数针对病毒性疾病的传统常规疫苗都是由在鸡蛋或哺乳动物的细胞培养物中生长的病毒制成的。通过收集病毒、使它们适应在实验室中生长,每种新疫苗都需要定制的生产过程,通过在生物反应器中生产常规病毒疫苗是一个成熟的过程,虽然漫长而繁琐,它包括种子病毒的制备、发酵、收获和纯化等几个步骤,可能需要几个月的时间。此外,处理大量的活病毒也是必要十分小心的。 所以常规疫苗就是注射抗原,即病毒的一部分,直接将抗原(一段病毒)注入体内。身体识别抗原(病毒)后,免疫系统会产生特异性抗体,当身体遇到病原体侵入时,特异性抗体就出来与入侵的病原体战斗。 常规疫苗的工作原理就是通过“训练”人体识别并对病毒或细菌等致病生物所产生的蛋白质作出反应。 
【信使核糖核酸 mRNA】 mRNA疫苗的工作原理则是,信使核糖核酸mRNA疫苗进入人体后会告知细胞制造SARS-CoV-2新冠病毒的特定部分:就是棘突蛋白。它是一种短时间存在的携带遗传信息的链状物质。 当信使核糖核酸 mRNA疫苗进入人体后,免疫系统会产生抗体 并激活T细胞(T细胞的英語:T cell、T lymphocyte)是淋巴细胞的一种,在免疫反應中扮演着重要的角色。T细胞会迅速破坏棘突蛋 白。 mRNA进入人体后的工作就是将生成抗原的遗传信息传递到细胞中的能制造蛋白质的细胞器那里。然后机体内的细胞将抗原送递回到细胞表面,然后触发所需的特异性免疫反应。如果,当遇到外界的实体病毒的入侵时,体内免疫系统会产生抗体并激活T细胞以破坏COVID-19 病毒的棘突蛋白。 mRNA疫苗是不需要病毒培植的,制造一批 mRNA 疫苗时基本不需要病毒。只用少量病毒用于初始基因测序和疫苗测试。 因此,与传统的常规疫苗相比,mRNA 疫苗本身不包含任何病毒蛋白,而只包含我们自己的细胞产生无害病毒特性所需的信息,从而触发所需的免疫反应,还可以解决潜在的新出现的有害病毒变种。 信使疫苗将COVID-19 病毒的无害小片段 编码并呈现 给免疫细胞,让免疫细胞“学习”了如何识别和攻击该病毒。当身体在接触实际病毒时能够产生快速和特异性的免疫反应 ,从而阻止病毒在人体的任何地方复制和传播。 信使核糖核酸 mRNA其实是非常脆弱的,它本身对人体没有任何的攻击性。医学科学家为了保护这种脆弱的分子能够顺利地潜入细胞,他们借助了一种比信使RNA疗法本身应用更早的传递技术:称为脂质纳米粒(lipid nanoparticles,简称LNPs)的微小脂肪球担任传递任务。 针对 COVID-19的冠状病毒在进入人类宿主细胞时,是由位于病毒表面的冠状病毒刺突蛋白导入的。当含有信使mRNA的脂质纳米粒(LNP)通过胞内体进入细胞时,将脂质纳米粒和信使RNA释放到细胞的细胞质中。一旦释放,信使mRNA就被核糖体化成蛋白质。 所以mRNA新冠核酸疫苗对注射到体内的COVID-19病毒无害的小片段送入免疫细胞中进行编码,让免疫细胞“学习”如何识别和攻击病毒。当机体接触到真正的病毒时,能够快速产生特异性免疫反应,从而防止病毒在人体内复制扩散及传染给其他人。所以 mRNA 疫苗就是为我们的身体提供代码,指导细胞识别棘突蛋白,让细胞机器帮助刺激自身免疫反应。免疫系统就会识别冠状病毒的表面的分子结构棘突蛋白,并能够将其消灭。 在此特别提示一下:这些疫苗中的 mRNA 只能进入细胞的某些部分,它无法进入细胞核。在上面关于细胞结构的部分里,我已经提到过,细胞核—主要内含遗传物质(即染色体、DNA、基因)。细胞核即我们自己的 DNA 所在的地方是不会受到任何干扰的。因为mRNA疫苗根本无法进入细胞核,所以它不会接触到我们的 DNA和基因。另外,它不会存活很长时间,也不会留存太久。它是非常脆弱的, 所以它在注入人体之前, 必须在超低温环境下储存疫苗,其原因也正在于此。它如果处于不稳定的温度中,就无法长时间保持稳定。它在进入人体和细胞几个小时后,便会开始产生这种棘突蛋白。我们的身体会在随后几天中对这种棘突蛋白做出反应,但这种信使m RNA 进入人体后不会到处游走,也不会进入我们的 其他器官。 当然,任何阶段性的疫苗都不是十全十美的,人类目前的医学研究还没有到达完美的境界,很多都在攻克阶段。

(卡塔琳·卡里科(Katalin Kariko)博士。(图片来自网络)
其实,信使核糖核酸 mRNA疫苗也不是什么新玩意,早在40几年前已经由科学家卡塔林·卡里科开始研发,后来多得她和医学家德鲁·韦斯曼,一直艰苦的坚持不懈的努力,在mRNA上的开创性工作为辉瑞和莫德纳的新冠疫苗铺平了道路。如果没有这项技术的奠基人——卡塔琳·卡里科(Katalin Kariko)博士的最后坚持,就没有今天拯救人类的Moderna疫苗。至今mRNA疫苗的研究已经走过了几十个年头,之前一直用在植物培植方面,近十几年用于癌症疫苗的研究,但一直没有用在活体的临床上。直到COVID-19大流行期间,这项技术才受到了人们的充分关注。与传统疫苗相比,mRNA疫苗引发的免疫响应更加平衡,能够触发特异性免疫系统的体液免疫和细胞免疫。虽然这一技术还没有正式获得美国FDA的上市批文,但从对抗COVID-19的相关产品的表现上看,mRNA疫苗表现出了巨大的可行性、安全性、有效性和快速发展的潜力。 所以,疫情最严重的时候,莫德纳的信使核糖核酸(mRNA)疫苗是一种还没有上市场的技术,后来美国联邦政府临危受命,批准使用抗 COVID-19 的莫德纳 mRNA-1273 疫苗。目的和策略明确强调由于 COVID-19 大流行在全世界造成了很高的发病率和死亡率,并导致严重的社会、教育和经济混 乱。因此,批准了【信使核糖核酸 mRNA】疫苗跨过临床审批的慢慢长路,直接进入市场,士急马行田,救人第一嘛。
我们谈到这里,小辈笑笑说:其实COVID-19的大流行把信使核糖核酸 mRNA疫苗提前推上了医学的殿堂,因为,世界上几亿人口来帮它做了临床。但是,事实证明,经过40多年的研究和在植物上面的应用,【信使核糖核酸 mRNA】疫苗是成功的稳定和有效的,如果现在还有人质疑的话,我觉得就没有必要了。 现在医学界已经将mRNA用在一种帮助摧毁癌细胞的疫苗上。截至目前,大多数利用mRNA诱发免疫反应的工作都集中在癌症领域,肿瘤mRNA被用来帮助人们的免疫系统识别并对特定肿瘤产生的蛋白质做出反应,告诉免疫系统的抗体和其他防御系统要搜索和攻击什么目标,癌细胞可以通过这种方式被摧毁。 mRNA全称为Messenger RNA——信使核糖核酸。在10月份德国生物技术公司BioNTech的创始人在接受BBC采访时称,mRNA新冠疫苗技术可用于帮助摧毁癌细胞,他说这意味着癌症疫苗可能在2030年前问世。 科学家认为,mRNA疫苗可能是解决大量疾病的关键,到时候不排除可以攻克更多恶性的疾病,特别是免疫系统方面的流行病。 好了,大家就不要再担心接种疫苗会改变基因的传言了,我们的染色体、DNA、基因都藏在细胞核里面,被人体严密保护着呢。 说明一下:这不是医学研究的专业文章,内容都是普通的医学常识。我只是想用最简单最通俗的演绎方法和语言与大家分享一下我对疫苗与细胞的认识,希望对各位读者有用处。 作者简介:张允遐,中国财经出版传媒集团合作作家,【滚滚红尘美利坚】作者。该书被中国各地图书馆和美国公共图书馆收藏。
|
