生命为什么会衰老? 假若时光可以穿越,让我带你回到38亿前去看生命的起源,相信你一定会……大失所望。当新生的地球刚刚冷却,一段被脂膜所包裹的RNA分子获得了自我复制的能力,地球生命就这样谦卑而蹒跚地迈出了进化的脚步。然而进化中的第一步却是无比的漫长和无趣。在最初18亿年进化中,无论是最初绽放出生命之芽的RNA生物体,还是后来居上的DNA为遗传信息的生命,星球的所有生物无不例外地仅以单细胞生命的形式,无聊无助地漂浮在远古海洋里……,直到有一天一个大个头的古菌体吞噬了一个小小的氧化菌。奇妙的是,吞噬没有成为“谋杀”,相反却演化出生命史中最重要的一次“联姻”。两个细菌建立了一个从所未有的新颖共生。大细菌给小细菌提供安全庇护,必要的蛋白和养分,甚至允许它保留自己的DNA可以在自己细胞里繁衍。而作为回报,小细菌则放弃了其他一切生命活动,“专职”利用氧气为大菌体和自己来制造能量,合成地球所有生命体最宝贵和必要的能量分子-ATP (三磷酸腺苷)。 正如同人类的财富需要转换成货币才能去使用,对于地球上所有的生命体而言,生命活动的所需能量也必须通过ATP分子形式来利用。于是当生命的细胞里开始拥有了这样的“能量印钞机”,地球生命进化才由此大步向前。只有从这时起,多细胞的生命才渐渐开始出现,生命的形式才由此变的精彩而复杂。在这之后的二十亿年,我们的星球才渐渐拥有了龙腾鱼跃的海洋,春暖花开的大陆;漫步或者飞翔的恐龙;以及今天低头玩手机的“智人“。 这个二十亿年前的”小细菌,就是人类以及所有真核细胞生物体细胞中的线粒体。今天它在你的细胞里已不再是个独立的生物体,但源自于独立细菌的特点依然清晰可见。比如,虽然作为细胞器,线粒体依然保留有自己的DNA,并在母体细胞需要更多能量时,也像寄生菌一样,对DNA进行复制,对自身进行分裂,繁衍出更多的线粒体。此外有趣的是,对于人类而言,线粒体的DNA仅通过母系遗传给后代。(父系的线粒体DNA在受孕时就被踢走了)这种简单的单系遗传也让今天的生物学家很方便的通过追踪线粒体DNA的突变,追踪到一位生活在大约20万年前南部非洲的女性,是今天人类所谓的“线粒体夏娃”。从线粒体DNA的遗传变异结果而言,今天所有人类都是可以看成是这位女性的后代。线粒体对生物体而言,它是不可替代的能量中心,是生命活动的引擎。我们生命中的每一次心跳,每一次呼吸,甚至大脑的每一个思考,所需要的能量几乎都由细胞中的线粒体来提供。如果全部折合分子ATP, 每个成年人每天的生命活动大致需要50-75公斤ATP所转化的能量。这些都要由你的每个细胞中成百上千的线粒体们在时时刻刻勤勉的制造。
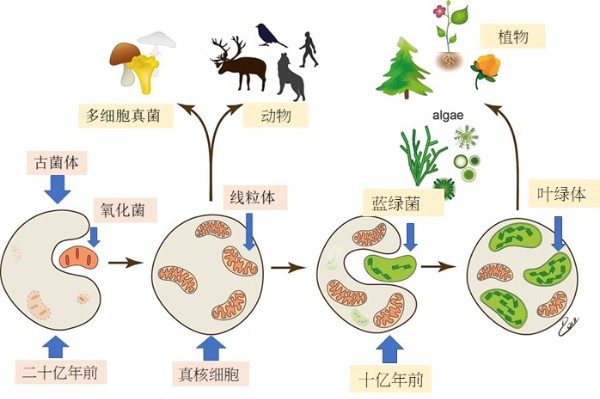
地球生命进化简图
虽然二十亿年前奠定下来的“一菌两制”成为地球今天所有高级生命的能量基石,也并非没有代价。 高级生命的衰老伏笔也由此埋下。在今天的衰老研究中,科学家无一例外地发现伴随着衰老的发生,各个组织器官中线粒体的都在发生着明显的变化。衰老的机体往往和细胞里破损,退化以及数量减少的线粒体在相互对应。虽然由于机体不同的细胞对能量的需求也不同,不同类细胞中线粒体的数量可以从几百到几千而不同。但随着机体的衰老,细胞中线粒体的相对数量可以观察到明显下降。而线粒体的结构,从DNA的完整到蛋白的结构也有明显的破损和退化。细胞中线粒体的差异实际上也是为什么一个青春少年总有无限精力,而一个耄耋老者总容易困倦疲乏的根本原因。 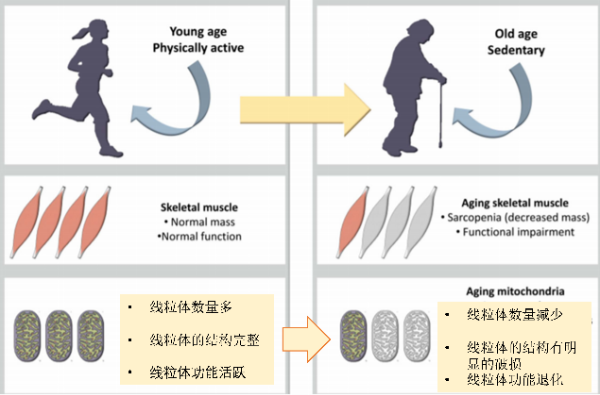
年轻人和老年人肌肉细胞中的线粒体比较
那么到底是线粒体的退化引起衰老,还是衰老本身导致线粒体的减少和退化呢?医学临床上一些线粒体遗传疾病为研究者们昭示了可信的证据和线索。比如,科学家发现有一类线粒体的遗传疾病称为MELAS (Mitochondrial Encephalopathy, Lactic acidosis, and Stroke 线粒体脑病)。这一类罕见线粒体缺损性的疾病常见于儿童,并在只有几岁的时候就开始发病。最初是肌肉的无力和疼痛。那是因为肌肉细胞往往是机体中对能量的要求是最多的。渐渐的患者的视力和听力如同衰老一样开始下降。这同样是由于缺乏能量,导致能量高需器官中的细胞开始渐渐消亡。然后患者逐渐开始有剧烈的头疼和癫痫,他们如同很多老年人一样,由于心脏肾脏,以及消化代谢功能的下降,可能会患上糖尿病。最后,这些儿童患者也如同老年人一样发展成失明,耳聋,甚至最后出现阿尔滋海默症。这些经常应该是老年性特有的疾病和症状却不幸过早地降临在这些儿童患者身上。这些先天性线粒体的缺损,无疑是这些衰老症状的元凶。事实上,科学家也注意到,机体中最先开始的衰老,往往也是那些对能量需求最高的器官,比如,肌肉,眼睛,心脏等。相信很多人正是从眼睛“老花”(眼肌无法完全收缩)开始对衰老有了第一个感觉。 正是基于这些研究和观察,美国科学家Denham Harman 最先所提出了所谓“线粒体致衰假说”并在科学界渐渐形成了一定的共识和支持。也就是说人体的衰老很大程度上是由细胞中线粒体的退化所引起。线粒体的退化,虽非唯一,但也至少是主要元凶。退化的起因依然可以追溯回二十亿年前生命史上那次看似完美的“一菌两制”的联姻。生命进化虽然由此飞跃。但其根本的设计缺陷,也让高级生命体的衰老成为某种必然。作为能量的制造者,线粒体在细胞中可以看成熊熊燃烧的火炉,勤勉不断的为母体细胞制造和输出着能量。这是个十分复杂而又时刻不能间断的过程。不仅有众多且容易出错的步骤,却也同时产生着大量破坏性很强的自由氧基(ROS),也正如温暖的火炉边,四溅的火星自然也难以避免。不幸的是,“火炉”边上正好放着“能量站”珍贵的图纸-线粒体DNA. 自由氧基遇到DNA这样脆弱的分子,其伤害不亚于四溅的火星对图纸的危险。公平的说自然界进化其实也早已“注意到”这个问题。在二十亿年的漫长进化中,线粒体的DNA已经被近可能的被压缩精简到很短。同人体细胞核里做拥三万多个基因段的母体DNA相比,线粒体的DNA实际上仅剩下37个基因段,负责编码着最基本的13个蛋白。看来为修补这个缺陷,自然进化真的也已经“尽力”了。 然而遗憾的是即使如此,自由氧基对线粒体的伤害依然不可能完全避免。衰老的脚步也由此跟随着生命时钟会缓缓迈开。针对DNA的伤害,人体细胞虽然也一套修复机制,但随着时光的推移,线粒体所产生的自由氧基对自身的DNA乃至蛋白的损害还是会不断地积累。细胞对DNA修补速度最终还是会渐渐无法赶上被这些不断产生的自由氧基所伤害的速度。当作为“制造蓝图”的线粒体DNA一旦因不可修补的损伤而开始丢失或突变,由此而衍生的下一代线粒体不仅会承传这些缺损和突变,而以此为“蓝图”所衍生的下一代线粒体的蛋白结构上也因此开始带上了缺损。更糟糕的是正如一个有缺陷的火炉,不会更温暖,但却会溅出更多的火星。而一个结构有缺损的线粒体不仅难以同等高效的制造能量,却会产生更多的自由氧基而对自身造成更多的伤害,从而让线粒体的不断缺损退化进入一种恶性的循环之中。从宏观的个体来讲,这也可以解释为什么,衰老往往开始总是缓缓的而来,最后却是在不断的被加速。
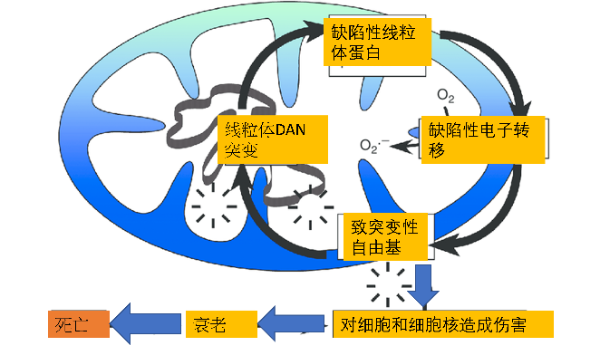
线粒体致衰理论示意图
逆转岁月的时钟
在08年奥斯卡最佳电影“本杰明_巴顿奇事”中有座逆向而转的大钟,是盲人钟表师为战争中逝去的年轻人特意而制。以此为背景主人公本杰明_巴顿从衰老走向青春的逆行人生的故事平行而精彩展开。现代生物学对线粒体和衰老的研究也让科学家们似乎窥见到了拨动人体岁月时钟的可能。线粒体致衰理论的启示下,科学家也自然意识到,想要拨慢甚至逆转人体衰老的岁月时钟,遏制线粒体的衰变或许为这样的梦想提供了一线希望。那么科学家们都在进行哪些尝试呢? 捕捉ROS 线粒体致衰理论中自由氧基是最直接的祸手。用抗氧剂来中和和捕捉线粒体内所产生自由氧基,是自然最先想到也是最容易的方法。近半个世纪以来,科学家设计了不同的各类实验,从实验室到临床对“抗氧延衰”的想法进行了严格的检验。然而遗憾的是近几十年的各类实验却表明,服用高剂量的抗氧剂对健康似乎并没有观察多大的好处,更谈不上延年益寿,在某些实验中甚至显示有害。原因何在呢?实际上大多数口服的抗氧剂,通过肠胃消化再经过血液的循环,能进入特定细胞却依然能保有一定的浓度和抗氧化性的分子寥寥无几。更不用说,在细胞中还需要再穿过另一层脂膜才能完全到达线粒体内。更诡异的是,在近20亿年的共存进化中,线粒体所产生的自由氧基在机体中居然也有了黑白两面性。一方面有破坏性,而另一面却又在很多细胞活动中,如基因的表达,免疫系统的应答等,扮演了重要调节的作用。有实验甚至表明有微量的自由氧基的存在,居然有助于延长实验动物的寿命。而过量的抗氧化剂则对所实验动物的健康和寿命有害。虽然当前的确还有少量的科学家在坚持探索更高效的抗氧剂来进行抗衰老研究。 “抗氧延寿”的观念现在更多的只是被的保健品商家所利用来赚取智商税。 假借的“上帝之手” 现代基因技术某种程度上像“上帝之手”改变着人类的社会。 那么能否能也用这样的“上帝之手”来拨慢岁月的时钟呢?生物学家们在尝试的另一类方法就是用基因技术来“修理”甚至替换细胞中的破损线粒体,正如同修理或者替换一辆旧车的发动机,而使之重焕青春。 方法之一是把需要替换的线粒体DNA重新注射到人体中,再通过某些生物技术的方法把它引入需要替换的细胞线粒体中。用这种方法,科学家们已经在实验室里可以成功的“修补”了因帕金森症而被损害的小鼠的脑细胞。另一个方法则是更加的逆天并且已昭示出了临床的希望。那就是希望通过基因技术把线粒体DNA的悉数都转移到细胞核中,即可以远离自由氧基的伤害又可以为线粒体的复制提供蓝图备份。前文已经提到, 在近二十亿年的自然进化中, 线粒体原有的大部分DNA已经精简压缩或被转移到母体细胞核中。科学家们在这里似乎希望完成自然进化所未能完成的事-把所有线粒体的DNA悉数转移到更安全的母体细胞核中,作为合成线粒体蛋白的“蓝图”备份。这近乎科幻的想法,最早在十年前就展示了突破。在实验小鼠上,科学家利用基因技术成功地把一段线粒体DNA基因引入到母体的细胞核并成功地把这一段人工注入的DNA转译成了对映的蛋白。用这种方法,科学家在小鼠模型上也成功地治疗了一种线粒体缺损性遗传病-Leber眼病。这类罕见疾病是由于线粒体DNA的遗传性缺损,导致线粒体的某些蛋白无法正常合成,而在人类身上则会引起致盲。于是在实验小鼠上,科学家先把这一类蛋白所相对应人工DNA利用基因技术引入母体细胞核中,并由让母体细胞成功转译合成这一线粒体所缺失的蛋白,这样的治疗在小鼠Leber眼病模型上显示出了良好的效果。经过科学家多年的努力和探索,一家总部在纽约名为GenSight Biologics生物科技公司在去年12月宣布展开了三期临床人体实验。虽然对Leber眼病患者而言无疑是个巨大的福音,对这项技术而言却只是“牛刀小试”。 重要的是可以潜在地成为是人类征服衰老的第一步。前文提到过线粒体DNA仅仅编译着13个蛋白。如果这一次临床实验顺利成功,这也意味着这个技术可以在理论上把线粒体所有DNA悉数人工转移到母体细胞核中。有了DNA“备份”在细胞核中,线粒体的退化会被有效节制,人体的衰老会被显著延缓。 脚下的“青春之泉” 在近几十年的抗衰老研究中有一些药物和行为目前已经被科学家所发现和证实,能在一定程度上减缓人类的衰老比如雷帕霉素,二甲双胍,以及禁食等。这些药物和行为虽然影响着机体不同的生理机制,但是它们都无不例外地参与着机体的能量代谢和调节。从某种意义上来讲,对机体能量的主要制造者-线粒体也应有着间接地保护,对减缓线粒体的退化也起着间接的贡献。此外在衰老的过程中,线粒体不仅有质的退化,也有量的减少。促进细胞线粒体的分裂和复制(biogenesis),在宏观上也是减缓机体衰老有效手段。科学家们惊讶地发现,达到这个目的,有一个简单的方法其实并不需要任何的药物或尖端技术,居然就是体育锻炼。科学家从不同的方面观察到,长期和一定强度的体育锻炼可以促进机体器官,尤其是高能量需求器官尤其是肌肉;大脑;心脏细胞中线粒体的复制和增生,明显地提高这些器官细胞中线粒体的数量。通过深入探索生物学家发现,运动的很大一部分生物功能是激活了人体一个掌控能量代谢重要生物信号通路-AMPK通路。。生物学上大部分的生物信号通路都如同蛋白的多米诺骨牌般复杂而精巧。AMPK通路也不例外。 在这个通路上起关键作用的蛋白是激酶AMPK。 它的激活会导致激活另一种名为PGC-1α的基因转译蛋白。正如其名一样,激活后的PGC-1α 进入细胞核对DNA上相应的基因进行转译,从而促使细胞合成另一类基因转译蛋白TFAM。最后在蛋白PGC-1α和TFAM共同作用下,又会对线粒体DNA也进行了相应的转译,从而激活并开启了线粒体的分裂和复制的信号。更有趣的是科学家还发现,运动和禁食居然可以激活机体同一个生物信号通路。也就是说运动和禁食这两种完全不同的行为,对机体的影响却有一定程度的相通。看来“管住嘴;迈开腿”似乎不仅是减肥的口号,或许也是长寿的秘诀。当然面对那些好吃懒做的人类,科学家们自然也不会袖手旁观。针对这生物机制的发现, 已经开始有科学家成立科技公司来试图寻找药物影响这一信号通路。试图不需挨饿,不必流汗 而是用药物地达到相同的目的。比如位于美国圣地亚哥的生物科技公司 Epirium Bio宣布自己已经有了初步的结果,并在吸引投资准备临床实验。不过在这遥远的的神药到来之前,今天最好的抗衰良药或许就是一双跑鞋。
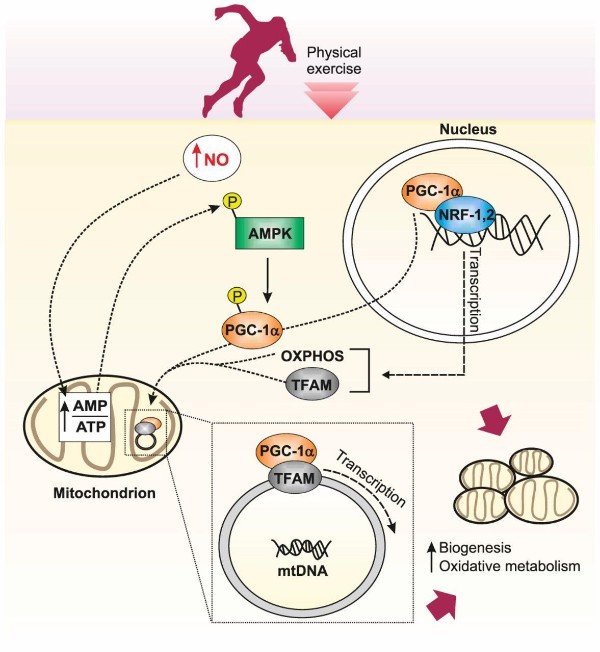
体育运动诱发细胞线粒体增生的生物机制
长达38亿年的生命长河中,在没有线粒体的前18亿年,生命是简单,无聊和无趣的。而只有当这个充满活力的“小细菌”共生到生命体中,进化才得以飞跃,生命才变得精彩。某种意义上讲,这一事件或许比生命起源来的更偶然和重要,虽然也给生命的衰老带来必然。不过窥见和理解了这一生命进化中的秘密,应当也为那些不懈寻觅青春不老泉的科学家们点亮了一盏小灯。我们或许可以憧憬着未来的“青春不老泉”,或许只是一针“线粒体重塑剂”-回春我们机体细胞中的线粒体。不仅延缓我们的衰老, 更憧憬的是可以让我们不论在何等年龄依然可以去精力充沛的享受生命,像家中十几岁的少年一样,可以在阳光下的网球场数小时地奔跑,可以在崎岖的山路上不知疲倦地骑上山巅……。最后值得一提的是最早提出线粒体致衰理论的美国科学家D. Harman。直到他八十多岁的时候,依然每天坚持着两英里长跑锻炼,健康地活到了九十八岁。看来无论是在理论还是实践这位可敬的科学家都已经为人类树立了榜样。
|
