中 續
接續:誰設計、製造了新冠病毒(二 中)
本文介紹其餘四篇furin酶切位點插入相關的病毒改造論文。
論文五
2008年9月10日,日本國立傳染病研究所的一組科學家在Journal of Virology上在線發表了如下論文:
Entry
from the Cell Surface of Severe Acute Respiratory Syndrome Coronavirus
with Cleaved S Protein as Revealed by Pseudotype Virus Bearing Cleaved S
Protein
帶有裂解S蛋白的假病毒揭示了帶有裂解S蛋白的SARS病毒的細胞表面進入(機制)
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2583654/
論文相關要點如下:
1、通過重疊PCR方法(基因改造、基因定點突變的最基本技術),將SARS病毒S蛋白第797~801氨基酸(殘基)由“KPTKR”替換為“KRRKR”,構建了S蛋白的人工切割突變體cl-S(cleavage-S)。引入的五氨基酸組合“KRRKR”中包含基本furin酶切組合“RRKR”。見下圖:
SARS(wild-type)S蛋白wt-S ,及其人工切割改造體cl-S結構示意圖
SARS病毒S蛋白S1亞基的最後一個氨基酸是R667(S蛋白的第667氨基酸R,R代表精氨酸R),在S蛋白第797氨基酸~801氨基酸之間設計、引入“KRRKR”或“RRKR”furin酶切位點位於S2亞基內,它將導致cl-S從第801氨基酸R801處被furin蛋白酶水解切割為兩部分(furin蛋白酶水解切割的位點是“RXXR”組合尾部的精氨酸R)。
2、將cl-S 、wt-S分別轉染入HeLa細胞和HeLa-ACE2細胞(即將兩種S蛋白的cDNA添加到細胞DNA中,使細胞DNA含有S蛋白基因),將細胞培養物孵育48 小時後發現:
a) cl-S 轉染的HeLa-ACE2細胞在不添加胰蛋白酶的情況下便可形成大的合胞體,而wt-S轉染的HeLa-ACE2細胞在不添加胰蛋白酶時不會形成合胞體;
註:cl-S可被細胞中廣泛存在的furin蛋白酶水解切割,其S2亞基的病毒-細胞,細胞-細胞膜融合能力因此被激活。
b) 如果在細胞培養基中添加胰蛋白酶(trypsin),那麼wt-S 轉染的HeLa-ACE2細胞也能形成合胞體;
註:SARS病毒S蛋白S1亞基的最後一個氨基酸R667是一個胰蛋白酶切位點,胰蛋白酶的水解切割也能激活S2亞基的病毒-細胞及細胞-細胞膜融合能力。
胰蛋白酶通常只存在於哺乳動物的小腸中,在其它細胞環境中並不存在;furin蛋白酶則在脊椎動物的各種器官、組織中廣泛存在,無須人為添加。
c) 無論是否添加胰蛋白酶,cl-S 或wt-S轉染的HeLa細胞(不含ACE2基因的Hela細胞)都不能形成合胞體(這表明,S1亞基與ACE2受體的結合是激活S2亞基膜融合能力,形成合胞體的先決條件)。
3、使用抗S2 兔血清進行蛋白質印跡分析,發現:
a) 在cl-S轉染的HeLa-ACE2細胞培養物中檢測到了分子量約為70 kDa的蛋白(它應是furin蛋白酶從R801處水解切割產生的S2亞基片段),在wt-S轉染的HeLa-ACE2細胞培養物中沒有檢測到這一片斷;
註:Da(Dalton,道爾頓)是分子質量單位,1Da=一個12C(碳12)原子質量的1/12;蛋白是大分子,其質量通常以kDa為單位(1kDa=1000Da);
完整的未切割的SARS病毒S蛋白的分子質量約為240kDa,S蛋白S1亞基的分子質量約為150kDa,S2亞基的分子質量約為100kDa。
b) 在添加胰蛋白酶的情況下,cl-S和wl-S轉染的HeLa-ACE2細胞培養物中都檢測到了分子量約為100kDa的蛋白(它應是胰蛋白酶從R667處水解切割產生的完整的S2亞基)。
c) cl-S轉染的不表達ACE2 的HeLa 細胞中未檢測到切割產物,也沒有檢測到細胞間融合。
2、3兩組實驗的結果如下圖:
在細胞中轉染表達的cl-S 和wt-S 的融合能力和可切割性
2、3兩組實驗表明:
a) S蛋白R801、R667兩個位點的蛋白酶(furin蛋白酶或胰蛋白酶)水解切割都能有效促成細胞-細胞融合形成合胞體(合胞體也稱多核擴大細胞或巨細胞);
b) (對SARS S蛋白而言)ACE2對誘導細胞間融合是必不可少的。
4、分別用wt-S、cl-S與VSV病毒(Vesicular Stomatitis Virus,水疱性口炎病毒)骨架嵌合,替代VSV的G蛋白,製作了兩種假病毒VSV/wt-S和VSV/cl-S。
VSV是彈狀病毒科(Rhabdoviridae)、水疱病毒屬(Vesiculovirus)的成員,病毒粒子為子彈狀或圓柱狀,它具有結構相對簡單、複製能力較強、發病過程快速、毒性、危險性低等特點,被廣泛用於研究RNA進化和製作假病毒。
G蛋白是VSV的囊膜糖蛋白,它的部分角色、功能相當於冠狀病毒的S蛋白。
下圖示意了將冠狀病毒的S蛋白嫁接到VSV病毒骨架上,替換掉其G蛋白製作假病毒的過程:
用VSV病毒、新冠S蛋白嵌合製作VSV-S假病毒示意圖
5、研究溶酶體抑製劑Baf(Bafilomycin,巴弗洛黴素)對病毒感染能力的影響。實驗證明:
baf使VSV/wt-S
對HeLa-ACE2 細胞的感染減少了90% 以上,但它只抑制了60%的VSV/cl-S
感染。研究者指出,他們製作的VSV/cl-S假病毒不純淨,其中混有相當數量的VSV/wt-S,baf對VSV/cl-S感染的抑製作用應該非常輕微。
由這一實驗結果可知,VSV/wt-S對HeLa-ACE2 細胞的感染嚴重依賴於溶酶體;而VSV/cl-S對HeLa-ACE2 細胞的感染則不依賴於溶酶體。
註:SARS病毒及帶有wl-S的VSV假病毒是通過內體途徑感染細胞的,病毒被內吞進入細胞後包裹在內體囊泡中,需要在內體中,或從內體運輸到溶酶體後,由溶酶體釋放的組織蛋白酶L對其S蛋白進行水解切割,激活S2亞基的膜融合能力,使病毒包膜與內體(囊泡)膜或溶酶體膜發生膜融合,並在膜融合後向細胞開放環境中釋放病毒包膜內的RNA(脫殼),完成感染過程,開始病毒複製。
VSV/cl-S有furin酶切位點,它可以被細胞內外廣泛存在的furin蛋白酶水解切割,而不必依賴於細胞內的溶酶體釋放的組織蛋白酶L的水解切割。如果cl-S的furin水解切割發生在細胞表面(完成受體結合後),那麼VSV/cl-S的病毒包膜可直接與細胞膜融合,並在二膜融合後立即向細胞內釋放RNA,第一時間開始病毒複製。這與新冠病毒的感染途徑是相同的,直接與細胞膜融合釋放RNA是最高效的感染方式,其效率是內吞方式的100~1000倍。再展示一下(直接)膜融合感染與內吞感染的對照圖:
新冠、SARS細胞感染生命周期(侵入、脫殼、複製、擴散)對照圖
6、研究幾種蛋白酶抑製劑對感染的影響。實驗證明,VSV/wt-S對HeLa-ACE2細胞的感染被三種CPL(cathepsin
L,組織蛋白酶L)抑製劑MDL、EST和leupeptin嚴重阻斷,而VSV/cl-S的感染只被部分抑制。這進一步表明,VSV/wt-S的感染高度依賴CPL,而
VSV/cl-S的感染則不依賴CPL。
5、6兩組實驗結果如下圖:
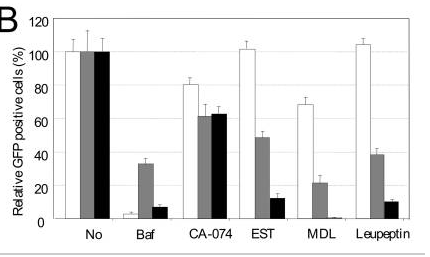
溶酶體抑製劑或組織蛋白酶抑製劑對病毒感染能力的影響
圖中,白色條柱對應G蛋白未被替換的VSV病毒,灰色條柱對應VSV/cl-S,黑色條柱對應VSV/wt-S;
VSV病毒或假病毒中都插入了GFP(Green fluorescent protein,綠色熒光蛋白)基因,並以GFP基因陽性細胞的數量來評估感染能力。以G蛋白未被替換的VSV病毒在未加抑製劑的情況下的感染能力為100%對照標準。
關於所使用的幾種抑製劑:
Baf是溶酶體抑製劑,可視為間接的CPL(組織蛋白酶L)抑製劑,CPL是溶酶體釋放的。
CA-074是組織蛋白酶B抑製劑;
EST、MDL是組織蛋白酶L抑製劑;
Leupeptin 是絲氨酸/半胱氨酸蛋白酶抑製劑。半胱氨酸蛋白酶包括組織蛋白酶B、H、L等,這意味着,Leupeptin同時是組織蛋白酶B、H、L的抑製劑。
還有一點要注意,如論文所述,VSV/cl-S中混有相當比例的VSV/wt-S,因此,VSV/cl-S感染的受抑製程度應該比結果圖顯示的情況輕得多。
論文指出,以上實驗結果(5、6兩組)共同表明:VSV/cl-S可以繞過內體途徑感染細胞,論文推斷,VSV/cl-S最有可能從細胞表面直接進入靶細胞(即指通過病毒包膜與細胞膜的膜融合直接從細胞表面向細胞內釋放病毒RNA)。
7、為了進一步證實VSV/cl-S
可直接從細胞表面進入,研究者聯合使用了溶酶體抑製劑Baf及一種七肽重複肽HRP(heptad repeat
peptide),後者(HRP)被證明(2007年10月的一篇論文)可以有效阻止
SARS病毒從細胞表面感染(指有外源性胰蛋白酶存在時,SARS病毒也可通過直接膜融合方式感染細胞),但不能阻止SARS病毒通過內體途徑感染。
在這組實驗中,Baf是內體途徑感染抑製劑,HRP是(細胞表面)直接膜融合途徑感染抑製劑。
實驗表明:
a) 只使用Baf時,與之前的實驗結果相同,VSV/wt-S對HeLa-ACE2細胞的感染被高度阻止,VSV/cl-S則保持了約40%的感染能力(其中可能混有60%的VSV/wt-S);
b) 只使用HRP時,VSV/wt-S的感染能力幾乎不受影響,VSV/cl-S則保持了約60%的感染能力(可能是其中混有的60%的VSV/wt-S造成的感染);
c) 當同時使用Baf和HRP時,不僅 VSV/wt-S的感染被高度阻止,而且VSV/cl-S的感染能力也幾乎盡失(VSV/cl-S的感染及其中混有的VSV/wt-S的感染都被強力阻斷)。
實驗結果見下圖:
Baf、HRP對VSV/cl-S、VSV/wt-S感染能力的影響
這表明:VSV/cl-S的細胞感染途徑,就是被HRP阻止的細胞表面直接感染途徑(病毒包膜在細胞表面與細胞膜直接融合併釋放病毒RNA)。
假病毒實驗結果預示着,擁有cl-S中furin酶切位點的SARS病毒變異體的感染途徑將與VSV/cl-S相同:不通過內吞,無須等到內吞後再與內體膜或溶酶體膜融合以釋放RNA,它的病毒包膜將在細胞表面與細胞膜直接融合,第一時間向細胞內釋放RNA。
具有cl-S中furin酶切位點的VSV/cl-S或SARS病毒變異體的感染方式就是新冠病毒的感染方式。
論文六
2009年3月24日,Cornell大學(康奈爾大學)獸醫學院微生物學與免疫學系的加里·惠特克(Gary R. Whittaker)領導的一個三人小組在PNAS(美國國家科學院院刊)上發表了如下論文:
Activation of the SARS coronavirus spike protein via sequential proteolytic cleavage at two distinct sites
經由兩個不同位點的連續蛋白水解切割(引發)的SARS 病毒刺突蛋白激活
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2660061/
https://www.pnas.org/content/106/14/5871
該研究在SARS病毒刺突蛋白中設計、引入了兩個furin酶切位點,其一在S1/S2處(R667處),其二在S2亞基內,S蛋白的第793~797氨基酸之間(與論文五的插入位置非常接近,這一位點通常稱為S2')。
S1/S2處的具體改造是,將SLLR之後的S蛋白第668~671氨基酸“STSQ”替換為“RSRR”,構建出了一個複合furin酶切組合“RRSRR”(與論文三SLLR變異體的構建非常相似)。改造前後的序列情況如下:
S1/S2處的序列改造情況
S2'處的的具體改造是,將S蛋白的第794~797氨基酸“PTKR”替換為“RTKR”(實際上只替換了一個氨基酸,把第794氨基酸由脯氨酸P替換為精氨酸R),構建了一個基本furin酶切組合“RTKR”。改造前後的序列情況如下:
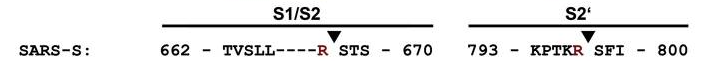
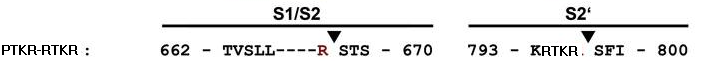
S2'處的序列改造情況
基於以上兩處改造,構建了三個SARS病毒S蛋白的人工變異(改造)體:SARS-Fur667、SARS-Fur797、SARS-Fur667-797。其中,SARS-Fur667和SARS-Fur797
各含一處改造,各具有一個furin酶切位點,SARS-Fur667-797同時包含二處改造,兼具兩個furin酶切位點。
實驗證明:
1、S1/S2處構建的furin酶切位點可使S蛋白被有效水解切割,裂解為分離的S1、S2亞基;
2、S1/S2處構建的furin酶切位點明顯增強了細胞-細胞融合,促進了合胞體的生成;
3、S1/S2處構建的furin酶切位點明顯提高了SARS病毒的非內體途徑感染效率。當在細胞培養物中添加了外源性胰蛋白酶時,帶有SARS
S蛋白及(S蛋白)變異體SARS-Fur667的MLV(Murine Leukemia
Virus,鼠白血病病毒)假病毒均可直接膜融合感染細胞,而且後者的感染效率顯著高於前者(216%±78%);
4、相比S1/S2位點,S2′處構建的furin酶切位點(對應變異體SARS-Fur797)的細胞-細胞融合、促成合胞體能力更為顯著;
5、兼具兩個furin酶切位點的變異體SARS-Fur667-797可導致超過95%的培養細胞發生細胞-細胞融合,形成非常大的合胞體。
SARS S蛋白(wt)及三種改造體細胞-細胞融合能力對照圖
論文七
2014年11月6日,荷蘭烏得勒支大學、萊頓大學、鹿特丹伊拉斯姆斯大學,瑞士蘇黎世大學、美國愛荷華大學的一組科學家在國際著名病原微生物學術期刊PLoS Pathogens上在線發表了如下論文:
Coronavirus Cell Entry Occurs through the Endo-_Lysosomal Pathway in a Proteolysis-Dependent Manner
冠狀病毒以依賴蛋白水解的方式通過內體/溶酶體途徑達成細胞進入
https://journals.plos.org/plospathogens/article?id=10.1371/journal.ppat.1004502
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4223067/
論文涉獵廣泛,內容博大,它對比研究了MHV-A59(鼠肝炎病毒A59株系)、FIPV(貓傳染性腹膜炎病毒)、MERS-CoV(中東呼吸綜合症冠狀病毒)、VSV(水疱性口炎病毒)、IAV(A型流感病毒)等等眾多冠狀病毒的細胞進入、感染途徑;它同時研究、考察了基因沉默(抑制、干擾特定的細胞基因),種種抑製劑、干擾劑(如RNA合成抑製劑、蛋白酶體抑製劑、內體成熟抑製劑、網格蛋白內吞介導抑製劑、肌動蛋白和巨胞飲作用影響劑、肌動蛋白細胞骨架改變劑、微管解聚誘導劑、膽固醇轉運影響劑等等)、內體PH值等五花八門的各種因素對各病毒細胞進入、感染的影響。
在研究MHV-A59的感染方式時,論文在其S蛋白S2亞基融合肽(FP,fusion
peptide)上游通過引入複合furin酶切組合,構建了一個MHV-A59的改造體MHV-S2‘FCS。具體改造是,通過定點誘變(site-directed
mutagenesis),將S蛋白的第865~ 869氨基酸“AIRGR”替換為“RRRRR”。見下圖A子圖:
MHV-A59改造體MHV-S2‘FCS的構建及CPI對病毒感染的影響
圖中的MHV-EFLM是在E蛋白(Envelope
protein,包膜蛋白)和M蛋白(Membrane protein,脂質膜蛋白)之間加入了FL(firefly
luciferase,螢火蟲熒光素酶)基因的MHV-A59;MHV-S2‘FCS因繼承了MHV-A59
S1/S2處原有的Furn酶切位點“RRAHR”而擁有兩個furin酶切位點。
實驗證明:
1、MHV-A59的感染能力取決於溶酶體蛋白酶對其S蛋白的水解加工(以激活S2亞基的膜融合能力,使病毒包膜與內體膜或溶酶體膜發生膜融合,並在膜融合之後向細胞中釋放RNA)。
2、當向Hela細胞中添加泛溶酶體蛋白酶抑製劑CPI時,MHV-A59的感染受到嚴重抑制。見上圖B子圖(以MHV -A59在不加CPI時的感染情況為100%對照標準)。
3、具有融合肽上游的弗林蛋白酶切割位點“RRRRR”的MHV-S2‘FCS不再需要從內體運輸到溶酶體,同時不再需要溶酶體蛋白酶對其S蛋白進行水解加工(它可在內體囊泡中先行被廣泛存在的furin蛋白酶水解加工),MHV-S2‘FCS的感染能力不受泛溶酶體蛋白酶抑製劑CPI的影響。見上圖B子圖。
4、添加furin蛋白酶抑製劑FI(furin inhibitor)顯著抑制了MHV-S2‘FCS對單倍體細胞HAP1的感染,當HAP1中缺乏VPS33A時,這種抑製作用更是表現得極為突出。見下圖:
FI可顯著抑制MHV-S2'FCS 的感染並增加其對內體~溶酶體成熟的依賴性。
註:
CPI:cysteine proteinase inhibitor,半胱氨酸蛋白酶抑製劑,亦稱胱抑素C,是一種泛溶酶體抑製劑。
HOPS :homotypic fusion and vacuole protein sorting,同型融合和液泡蛋白分選,一種細胞中的蛋白複合體,參與晚期內體到溶酶體的成熟。
VPS33A,是HOPS一個重要亞基。
HAP1是一種近單倍體細胞系,它象永生的癌細胞系那樣可以無限期分裂,並且幾乎每個細胞都只有一個染色體拷貝。
H1-ΔV33是敲除了VPS33A亞基基因的HAP1細胞。
H1-ΔV33-fV33是先敲除VPS33A基因,再添加帶有FLAG的VPS33A基因得到的HAP1細胞。
5、MHV-S2'FCS仍然是通過內吞途徑感染細胞的,但其病毒包膜與內體囊泡膜的膜融合發生在早期內體階段(膜融合後病毒RNA得以脫殼釋放到細胞開放環境中開始病毒複製);相比之下,MHV-A59的膜融合及RNA脫殼則發生在晚期內體階段或溶酶體中(內體運輸到溶酶體或內體與溶酶體結合)。MHV-S2'FCS的感染效率顯著高於MHV-A59。
論文其它內容我就不贅述了,用論文的一個概括性配圖來結束對該論文的介紹:
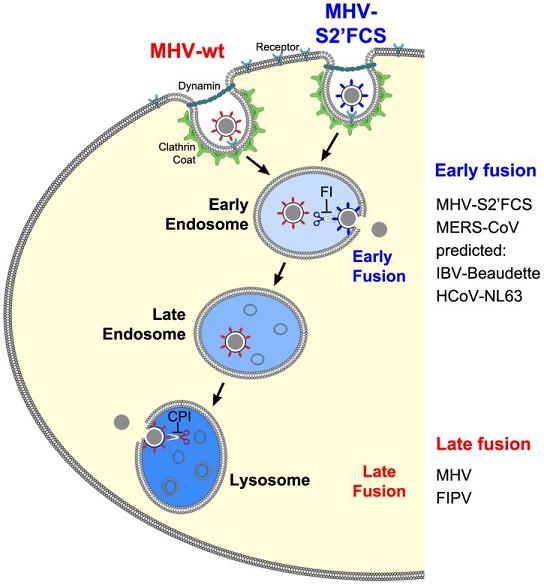
冠狀病毒內吞感染的早期融合與晚期融合模型
論文八
中國科學家也做過furin酶切位點插入研究、實驗。下面是我找到的唯一一個例子,一個很晚的例子。
2019年10月22日,中國農業大學獸醫學院,農業部動物流行病學重點實驗室的一組學者在MDPI(Multidisciplinary Digital Publishing Institut,多學科數字出版機構)旗下的Viruses月刊在線發表了如下論文:
The S2 Subunit of QX-type Infectious Bronchitis Coronavirus Spike Protein Is an Essential Determinant of Neurotropism
QX型傳染性支氣管炎冠狀病毒刺突蛋白的S2亞基是嗜神經性的基本決定因素
https://www.mdpi.com/1999-4915/11/10/972
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6832359/
該研究的核心實驗結論是:
在S2' 處引入furin酶切位點獲得的重組QX基因型(QX型)傳染性支氣管炎病毒(IBV)導致更強的致病性、明顯的神經症狀和嗜神經性,它能破壞血腦屏障,誘發嚴重的腦炎並導致更高的死亡率。
傳染性支氣管炎病毒(Infectious Bronchitis virus,IBV)是一種γ譜系(丙型冠狀病毒屬)冠狀病毒(新冠、SARS、MERS是β譜系,即乙型冠狀病毒屬冠狀病毒),發現於1930年,是最早發現的冠狀病毒。
IBV能引發家禽的傳染性支氣管炎,雞是IBV的最主要感染對象;IBV的侵害部位包括(雞)的呼吸道、生殖道(如輸卵管),以及腎臟、腸道、腺胃(前胃)等眾多內臟器官,並可在內臟器官中持續存在160天;IBV的感染致死率約為15%~30%,小於10日齡的雌性雛雞感染IBV往往導致永久性輸卵管損壞。
IBV包括數百個血清型或毒株型,QX(Qingdao
Xianwei)型IBV是IBV的一個腺胃型分支,最早發現、分離、鑑定於中國青島地區(1999年),它在世界範圍內廣泛流行,也是中國2013年後最具流行優勢的IBV類型。QX型IBV感染損害雞的呼吸系統、消化系統和泌尿生殖系統,引發腺胃炎、腎炎等多種症狀。QX型IBV對呼吸道黏膜造成嚴重損傷,使病雞容易受到支原體、細菌或其他病原體的繼發感染,死亡率很高。
論文的研究樣本是IBV-YN,一種QX型IBV毒株,收集於2005年。研究者製作了IBV-YN的感染性克隆毒株IBV-rYN(簡稱為rYN),同時製作了一個IBV-YN的人工變異體(改造體)IBV-rYN-S2/RRKR(簡稱為rYN-S2/RRKR),rYN-S2/RRKR在IBV-YN
S蛋白S2亞基融合肽(FP)上游的S2'處(第695氨基酸處)引入了一個furin酶切位點。具體改造是,將S蛋白第692~695氨基酸由“PRGR”替換為“RRKR”。rYN-S2/RRKR繼承了IBV-YN
S1/S2處原有的複合furin酶切位點“RRFRR”(第538~542氨基酸)。見下圖:
在IBV S蛋白S2亞基FP上游S2'處引入furin酶切位點示意圖
實驗證明:
1、rYN-S2/RRKR對10天大的SPF胚蛋的致病能力、致命性顯著增強。
a) rYN-S2/RRKR接種導致所有SPF含胚卵在接種後36 小時(hpi,hours post of the infection) 內全部死亡,相比之下,rYN則需要超過96 小時;
b) rYN-S2/RRKR 的50% 胚胎感染劑量(EID50 ,50%Embryo Infectious Dose)) 僅為rYN的十分之一;
c) 不過,rYN-S2/RRKR 的50% 組織培養感染劑量 (TCID50 ) 比rYN 高1000倍以上,rYN-S2/RRKR在CEK細胞(Chicken embryo kidney,雞胚腎細胞)的複製相比rYN顯著減少。
註:SPF指Specific Pathogen Free,即無特定病原;SPF雞或SPF蛋指不含國際規定的19種病原體和相關抗體的雞或雞蛋;SPF 胚蛋,指用SPF 雞蛋孵化到一定日齡的內有活的胚胎的雞蛋;
2、rYN-S2/RRKR 顯著增強了對雛雞的致病能力、致死率
a) 用一日齡SPF雛雞進行感染致病實驗。
接種(眼內接種)rYN 菌株的1日齡SPF雛雞在接種後第5天(dpi,days post of the infection) 開始出現打噴嚏和無精打采的臨床症狀。在14天的實驗觀察期內有1隻雛雞死亡(每個觀察組10隻小雞),死亡率為10%;
rYN-S2/RRKR接種組的雛雞出現腹瀉臨床症狀和意外的神經系統症狀,如頭部震顫和癱瘓。該接種組第4天出現雛雞死亡,在觀察期內,該組10隻小雞中有9隻死亡,死亡率為 90%。
一日齡雛雞感染、致病、存活實驗結果
圖中control組指未接種病毒的10隻一日齡小雞。
b) 用3周齡SPF小雞進行感染致病實驗。
接種rYN 菌株的3周齡小雞在接種後第11天開始表現出無精打采,一隻小雞在第13天時死亡,死亡率為10%;
接種rYN-S2/RRKR的3 周齡小雞在接種後第8天時開始出現頭部震顫的神經症狀,但沒有麻痹。兩隻3周齡小雞分別在第9天和第13天死亡,死亡率為20%。
3周齡小雞感染、致病、存活實驗結果
3、解剖發現,
a)
rYN和rYN-S2/RRKR均對1日齡雛雞的呼吸和泌尿系統造成了嚴重損傷(rYN-S2/RRKR對腎的損傷略輕於rYN),但只有rYN-S2/RRKR造成了顯著的CNS(central
nervous
system,中樞神經系統)損傷,例如大量小膠質細胞增生、形成小膠質細胞結節,血管周圍發生炎性浸潤等(神經膠質細胞是血腦屏障的構成要素)。
rYN 、rYN-S2/RRKR對一日齡雛雞氣管、腎、大腦的損傷對比
圖中縱坐標代表病變嚴重程度評分:0 = 無顯微損傷,1-3 = 輕度損傷,4-6 = 中度損傷,7-10 = 嚴重和廣泛損傷。
線段上的“*”號代表線段端點對應的兩組數據的差異程度,“*”號越多表示兩組數據差異越大(該圖是用GraphPad Prism7.5繪製的)。
一日齡雛雞大腦病變、損傷的染色腦切片顯微鏡圖像
左上子圖對應控制組小雞(未接種病毒的小雞);左下對應接種rYN的小雞;中上顯示了接種rYN-S2/RRKR的小雞大腦中的大量小膠質細胞增生,及一個相當大的小膠質細胞結節;中下顯示了接種rYN-S2/RRKR的小雞大腦中血管周圍的炎性浸潤;右上、右下分別是中上、中下的局部放大圖。
b) rYN-S2/RRKR對3周齡小雞呼吸和泌尿系統的損傷明顯輕於rYN,但仍對CNS造成嚴重損傷,在rYN-S2/RRKR接種組的3周齡小雞大腦中仍然檢測到大量的小膠質細胞增生和血管周圍炎症浸潤。
rYN 、rYN-S2/RRKR對3周齡小雞氣管、腎、大腦的損傷對比
3周齡小雞大腦病變、損傷的染色腦切片顯微鏡圖像
左上子圖對應控制組小雞(未接種病毒的小雞);左下對應接種rYN的小雞;中上顯示了接種rYN-S2/RRKR的小雞大腦中的大量小膠質細胞增生;中下顯示了接種rYN-S2/RRKR的小雞大腦中的血管周圍炎性浸潤;右上、右下分別是中上、中下的局部放大圖。
論文指出:
血管周圍炎性浸潤表明,rYN-S2/RRKR感染能破壞、突破血腦屏障(BBB,blood–brain barrier),損傷中樞神經系統(CNS),導致重症腦炎;重症腦炎是rYN-S2/RRKR感染死亡率高於rYN的原因所在。
不過,rYN-S2/RRKR雖然增強了對不同日、周齡SPF小雞的致死力,新獲得了損傷神經系統的能力,但它同時減少了對小雞呼吸系統和泌尿系統的損傷。
4、
IHC(Immunohistochemistry,免疫組織化學檢查)結果顯示,rYN接種組小雞腎中的IBV抗原(antigen)陽性細胞多於rYN-S2/RRKR接種組;rYN-S2/RRKR接種組小雞大腦中有大量IBV抗原陽性細胞,而rYN接種組大腦中沒有IBV抗原陽性細胞。這些檢查結果表明:rYN-S2/RRKR變異體在小雞體內降低了上皮嗜性,但表現出神經嗜性。
論文指出,引入furin-S2'位點的IBV-YN改造毒株rYN-S2/RRKR的神經嗜性,在IBV中從未報道過。
小雞腎、腦切片中的抗原陽性細胞顯微圖像
小雞腎、腦切片顯微鏡視野中每個切片的陽性細胞數
0 = 無陽性細胞,1 = 1-10 個陽性細胞,2 = 11-30 個陽性細胞,3 = 31-50 個陽性細胞, 4 = > 50 個陽性細胞。 腎臟中rYN陽性細胞多於rYN-S2/RRKR,而rYN和陰性對照組(控制組)的腦中均沒有陽性細胞。
5、QX型IBV 疫苗SZ130(一種QX型IBV減毒株和IBV候選疫苗)仍可提供針對rYN和rYN-S2/RRKR的有效保護。
先接種SZ130,兩周后分別接種rYN或rYN-S2/RRKR的兩組各10隻一日齡雛雞觀察期內無一死亡,而且沒有出現任何臨床症狀(接種rYN或rYN-S2/RRKR後的觀察期為兩周)。
(未完待續)
|
