接续:“万能”受体适配器--新冠S蛋白 1
5、HS/HSPG
HS:heparan sulfate,硫酸乙酰肝素,是一种带高负电荷的高酸性链状多糖,也是一种硫酸化的糖胺聚糖(glycosaminoglycans,GAGs)。
HS在人类和动物组织中普遍存在,它可能存在/表达于人和哺乳动物所有细胞类型的表面,以及细胞外基质和基底膜中。HS具有非凡的结构多样性,能够与各种蛋白、多肽相互作用并发挥不同的功能。HS可与免疫系统的多种成分相互作用,如与多种细胞因子及某些T细胞受体结合,在免疫系统中发挥多方面的重要作用。HS已被证明可以调节白细胞发育、白细胞稳态、白细胞迁移,参与T细胞共刺激、免疫激活和炎症过程。HS还可能调节免疫突触中关键成分的可用性,并在信号传导、细胞间通讯中发挥作用。
HS通常附着在各种核心蛋白上形成HSPG(heparan
sulfate
proteoglycans),即硫酸乙酰肝素蛋白聚糖,或称为HS-蛋白聚糖(HS-proteoglycans)。在HSPG中,核心蛋白与HS多糖链通过共价键连接,一个核心蛋白可连接1个、2个或3个HS多糖链。HSPG能够通过结构异常多样的HS链结合大量配体,包括生长因子、形态发生素、细胞因子、趋化因子、酶、基质蛋白,以及细菌和病毒等病原体。HSPG通过广泛的结合能力在多种细胞过程中发挥关键(调节)作用,如细胞粘附、受体激活、细胞骨架组装、细胞外基质重塑、内吞作用、细胞间串扰、信号传导、感知组织损伤和介导炎症反应等等。
总之,HS/HSPG在组织内普遍表达且功能丰富,在众多生理、病理过程中发挥重要作用,二者的很多生理、病理作用等同或高度相关。
HS/HSPG是多种病毒的感染受体或附着因子,这些病毒包括:HIV(艾滋病病毒,属于逆转录病毒科慢病毒属)、HSV-1/2(herpes
simplex virus
1/2,单纯疱疹病毒血清型1/2,二者属于疱疹病毒科)、HCoV-NL63(人冠状病毒NL63,属于冠状病毒α谱系,新冠属于β谱系)、HCV(hepatitis
C virus,丙型肝炎病毒,属于黄病毒科肝炎病毒属)、HRSV(Human Respiratory Syncytial
Virus,人类呼吸道合胞病毒,属于副黏液病毒科肺病毒属)、Sindbis
virus(SINV,辛德比斯病毒,属于披膜病毒科甲病毒属,一种由蚊子传播的分布最广泛的虫媒病毒)、MCPyV(Merkel cell
polyomavirus,默克尔细胞多瘤病毒,属于多瘤病毒科,一种罕见的高恶性皮肤癌的致病因)等等。SARS-CoV-1也有一定程度的HS/HSPG结合能力,但HS/HSPG可能干扰而不是促进SARS-CoV-1的感染。
在SARS-CoV-2感染中,HS/HSPG是ACE2的共受体/辅助受体,可显著促进ACE2依赖性感染。在感染细胞时,SARS-CoV-2的S蛋白会同时结合ACE2和HS/HSPG。
论文依据一
SARS-CoV-2 Infection Depends on Cellular Heparan Sulfate and ACE2
SARS-CoV-2感染依赖于细胞硫酸乙酰肝素和ACE2
https://www.cell.com/cell/fulltext/S0092-8674(20)31230-7
论文“Highlights”部分(译文):
a)SARS-CoV-2刺突蛋白通过RBD与硫酸乙酰肝素和ACE2相互作用;
b)硫酸乙酰肝素促进SARS-CoV-2 Spike-ACE2相互作用;
c)SARS-CoV-2感染共同依赖于硫酸乙酰肝素和ACE2;
d)肝素和非抗凝衍生物可阻断SARS-CoV-2结合和感染。
论文具体要点:
1、SARS-CoV-2 Spike(刺突蛋白、S蛋白)通过RBD(Receptor Binding Domain,受体结合域)与硫酸乙酰肝素及ACE2相互作用,单个RBD可以在细胞表面同时结合HS和ACE2。
2、分析表明,SARS-CoV-2 RBD与HS的结合能力,显著强于SARS-CoV-1(SARS-CoV)RBD与HS的结合能力。如下图所示:
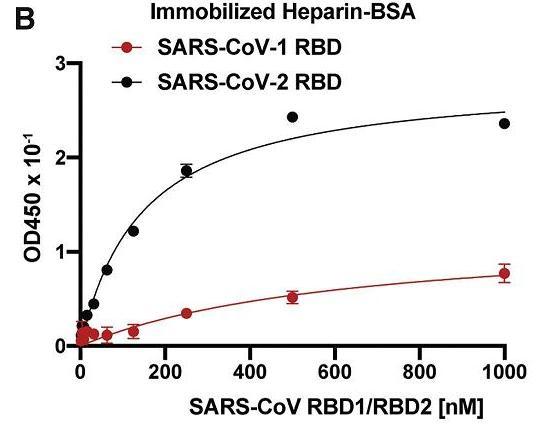
SARS-2 RBD、SARS-1 RBD的HS结合能力对照
SARS-2代表SARS-CoV-2。
BSA ,Bovine Serum Albumin,牛血清白蛋白。Immobilized heparin-BSA为牛血清白蛋白培养液中的固定化肝素。
heparin(肝素)是肥大细胞(Mast
cell)和嗜碱性粒细胞(basophil cells)的分泌物,最早是从动物肝脏中分离、发现的。heparin(肝素)、heparan
sulfate(硫酸乙酰肝素)都是硫酸化的糖胺聚糖,它们的结构非常相似,heparin也能结合SARS-2、SARS-1的RBD,但它不是一种细胞膜受体。heparin可作为与HS竞争SARS-2
S/RBD的干扰、抑制剂。
3、SARS-CoV-2 HS结合能力的显著提升,是通过两个氨基酸替代Thr444Lys和Glu354Asn获得的。
这意味着,基于SARS-CoV-1不难获得SARS-CoV-2的HS结合能力。有必要对此多做一些说明(无须研究技术细节的读者可跳过)。
三字母缩写Thr代表苏氨酸(Threonine),其单字母缩写为T,即Thr=T;Lys代表赖氨酸(Lysine),其单字母缩写为K,即Lys=K。替代Thr444Lys=T444K。
Glu代表谷氨酸,其单字母缩写为E,即Glu=E;Asn代表天冬酰胺,其单字母缩写为N,即Asn=N。替代Glu354Asn=E354N。
关于20种常见氨基酸及缩写,可参阅:
氨基酸 – 维基百科,自由的百科全书.htm
https://zh.wikipedia.org/zh-hans/%E6%B0%A8%E5%9F%BA%E9%85%B8
前面的氨基酸对应SARS-CoV-1,后面的氨基酸对应SARS-CoV-2,中间的数字是SARS-CoV-2 S蛋白氨基酸序列的序号。
替代Thr444Lys(T444K)表示,相对SARS-1,SARS-2
S蛋白的第444氨基酸位点发生了从苏氨酸(T,Thr)到赖氨酸(K,Lys)的替代或突变。或者说,SARS-2
S蛋白氨基酸序列的第444氨基酸是赖氨酸(K,Lys),而这一位点在SARS-1
S蛋白对应位点处的氨基酸是苏氨酸(T,Thr)。由稍后的附图可知,SARS-2 S蛋白第444氨基酸对应SARS-1 S蛋白第431氨基酸。
同理,替代Glu354Asn(E354N)表示,相对SARS-1,SARS-2 S蛋白的第354氨基酸位点发生了从谷氨酸(E,Glu)到天冬酰胺(N,Asn)的替代或突变。SARS-2 S蛋白第354氨基酸对应SARS-1 S蛋白第341氨基酸。
由“SARS-CoV-2 HS结合能力的显著提升,是通过两个氨基酸替代Thr444Lys和Glu354Asn获得的”这一判定可知:
a)如果SARS-1 S蛋白第341氨基酸由谷氨酸(E,Glu)突变为天冬酰胺(N,Asn);同时,第431氨基酸由苏氨酸(T,Thr)突变为赖氨酸(K,Lys),那么,SARS-1就能演化出与SARS-2相同或相当的HS结合能力。
b)如果用天冬酰胺(N,Asn)替换SARS-1 S蛋白第341氨基酸谷氨酸(E,Glu);同时,用赖氨酸(K,Lys)替换第431氨基酸苏氨酸(T,Thr),那么,就基于SARS-1改造出了一种HS结合能力与SARS-2相同或相当的新型冠状病毒。
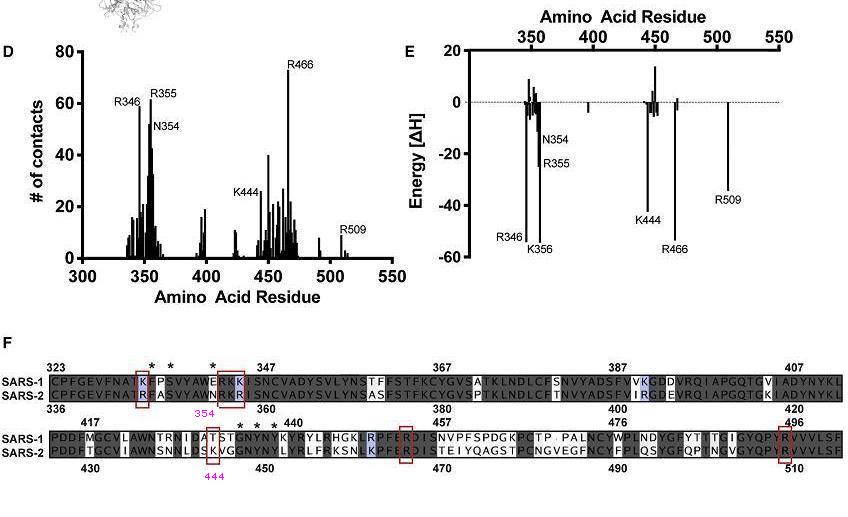
对结合HS贡献高的SARS-2氨基酸残基及对应的SARS-1氨基酸残基
不妨再说明一下这两个替代发现、确认的过程:
1)研究者首先找出了对结合HS贡献高(包括接触数贡献和能量贡献)的SARS-2氨基酸残基,上图用红色方框标出了这些残基(E354N处亦应有红框)。
2)接下来比较高贡献氨基酸与SARS-1中的对应位点氨基酸。一部分高贡献氨基酸与SARS-1中对应位点氨基酸相同,只有四个高贡献氨基酸与SARS-1中对应位点氨基酸不同,四组差异氨基酸是K346R、K357R、E354N、T444K。
3)四组差异氨基酸中的前两组K346R、K357R都是赖氨酸K到精氨酸R的保守替换。赖氨酸、精氨酸都是碱性残基,二者物理、化学性质接近,它们之间的替换对HS结合能力影响不大。
4)因此,对SARS-2 HS结合能力提升起关键作用的是另外两组差异氨基酸,即替换E354N、T444K,也就是Glu354Asn、Thr444Lys。
4、SARS-2 RBD在开放构象(RBD-Up)和闭合构象(RBD-Down)下皆可结合HS,在开放构象下HS结合亲和力更高;SARS-2 RBD只能在开放构象下结合ACE2。如下图所示:
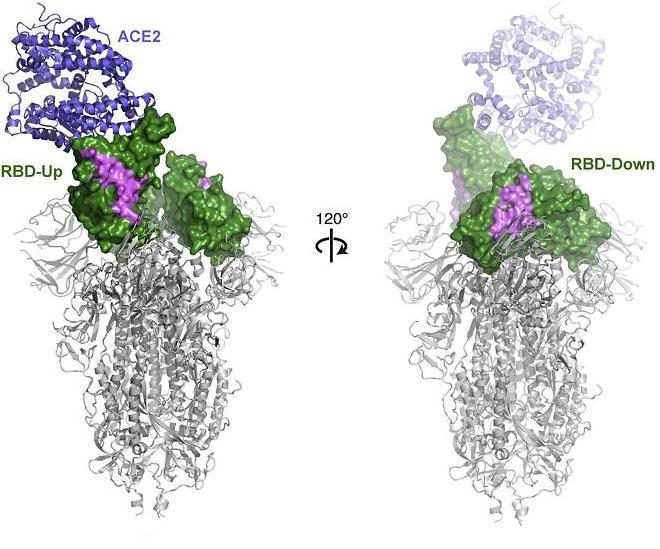
SARS-2 RBD在开放构象、闭合构象下皆可结合HS,但只能在开放构象下结合ACE2
图中绿色部分表示HS,紫色部分表示SARS-2 RBD与HS的推定结合区域。
5、ACE2不与HS结合,ACE2不影响SARS-2 Spike与HS的结合。
6、SARS-2 Spike可以分别结合ACE2和HS,也可以同时与二者结合,并以肝素为支架生成三元复合物;RBD的HS结合位点与RBD的ACE2结合位点相邻。
7、HS提升了S(Spike)蛋白的ACE2结合效率。与ACE2结合的S蛋白数量,随着S蛋白与HS的结合成比例地增加;电子显微照片成像研究表明,RBD与HS的结合可以形成有利于结合ACE2的开放构象,可以稳定RBD与ACE2的相互作用,增加与ACE2结合的Spike比例,并提高单个Spike结合ACE2的利用率(一个Spike三聚体可以结合1~3个ACE2)。这些情况表明,HS作为辅助受体启动、促进了SARS-2
Spike与ACE2的相互作用与结合。
8、用肝素裂解酶HSase(可裂解、降解细胞表面的HS)预处理细胞培养物,显著抑制了SARS-2 Spike、RBD肽与两种人类肺细胞H1299、A549,以及与人类肝细胞Hep3B、人类黑色素瘤细胞A375的结合。如下图所示:
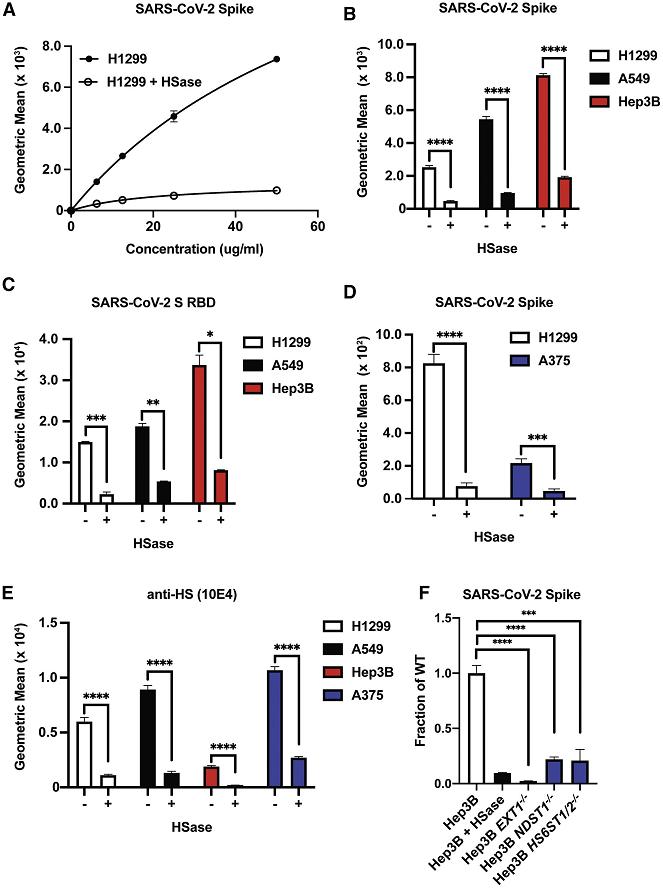
HSase有力抑制了SARS-2 Spike、RBD的多种细胞结合能力
H1299细胞:一种源自2型肺泡细胞的人类肺腺癌(非小细胞肺癌)细胞系,有说H1299 细胞摘取自淋巴结;
A549细胞:另一种2型人类肺泡腺癌细胞系;
Hep3B细胞:一种人肝癌细胞系;
A375细胞:一种人恶性黑色素瘤细胞系。
9、用HSase预处理细胞培养物,及敲除细胞中的EXT1、NDST1、HS6ST1/2等合成HS所需的生物合成酶基因都非常显著地抑制了SARS-CoV-2 Spike、RBD与Hep3B细胞的结合。如上图F及下图所示:
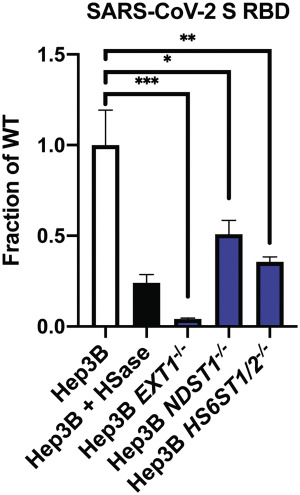
使用HSase,敲除EXT1、NDST1、HS6ST1/2显著抑制SARS-2 RBD的细胞结合能力
EXT1:Exostosin-1,与另一基因EXT2编码合成HS主链所需的糖基转移酶;
NDST1:N-Deacetylase And N-Sulfotransferase 1,N-脱乙酰酶和N-磺基转移酶1,一种HS中心修饰酶(催化硫酸盐与碳水化合物的结合,催化硫酸盐从3'-磷酸腺苷-5'-磷酸硫酸盐转移到HS中葡萄糖胺的氮);
HS6ST1/2:heparan
sulfate
6-O-sulfotransferase1/2,硫酸乙酰肝素6-O-硫酸转移酶1/2,两种HS合成修饰酶(功能类似NDST1,可将腺苷3'-磷酸-5'-磷酸硫酸中的硫酸盐基团催化转移到HS中N-磺基葡萄糖胺的第6个残基位点)。
“-/-”表示敲除了相应基因,例如,Hep3B EXT1-/-是敲除了EXT1基因的Hep3B细胞。
10、用提取自人类肺脏、肾脏、肝脏和扁桃体的HS(硫酸乙酰肝素)预处理细胞培养物,都显著抑制了SARS-2
RBD与H1299细胞的结合(下图B。外源性HS结合、消耗了SARS-2 RBD/Spike,被外源性HS占位结合的RBD/Spike
不能再结合细胞表面的HS);用多种外源性Heparin(肝素)/HS预处理细胞培养物,都显著抑制了SARS-2
Spike与H1299细胞(下图C)、与A549细胞(下图D)的结合。
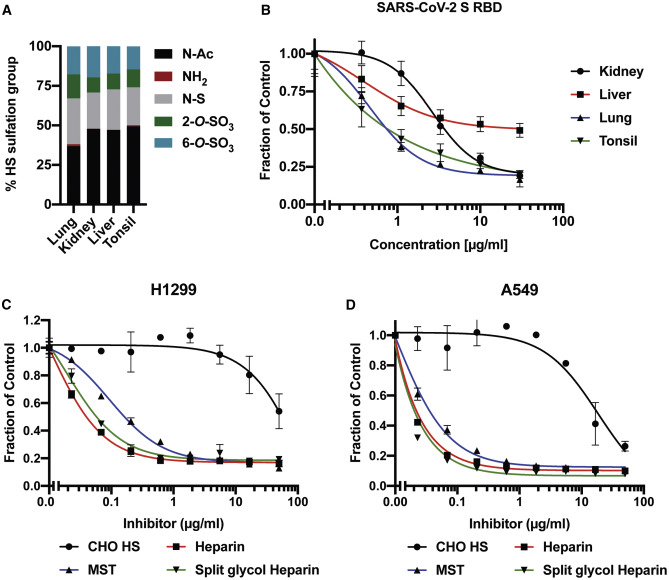
图B:四种提取来源的外添加HS显著抑制了SARS-2 RBD与H1299细胞的结合;
图C:CHO HS、Heparin、MST、Split glycol Heparin显著抑制了SARS-2 Spike与H1299细胞的结合;
图D:CHO HS、Heparin、MST、Split glycol Heparin显著抑制了SARS-2 Spike与A549细胞的结合。
CHO HS:提取自中国仓鼠卵巢的HS(硫酸乙酰肝素)。CHO:Chinese hamster ovary,中国仓鼠卵巢;
Heparin:肝素;
MST:指MST heparin,提取自MST(murine mastocytoma,小鼠肥大细胞瘤)细胞的肝素;
Split glycol Heparin:裂解乙二醇肝素/乙二醇裂解肝素。
11、ACE2过表达(通过ACE2基因转染)显著提升了SARS-2 Spike与A375细胞的结合(下图B);
用肝素裂解酶HSase预处理细胞培养物、敲除细胞中的糖胺聚糖组装基因B4GALT7显著抑制了SARS-2 Spike与A375细胞的结合(下图B);
敲除ACE2显著抑制了SARS-2 Spike与A549细胞的结合(下图C);
用肝素裂解酶HSase预处理细胞培养物显著抑制了SARS-2 Spike与A549细胞的结合(下图C);
这些结果表明,SARS-2 Spike与细胞的结合同时依赖于ACE2和HS。
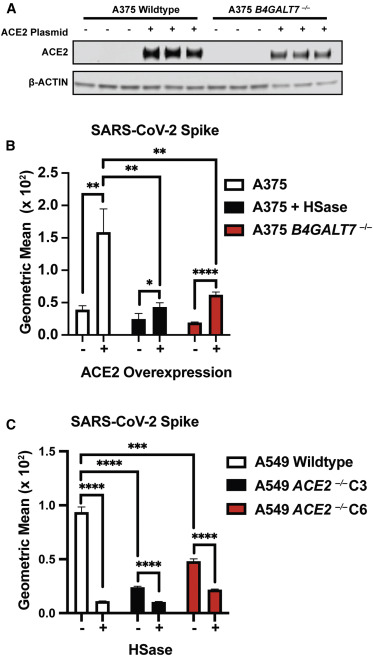
A375 B4GALT7-/-是敲除了B4GALT7基因的A375细胞;
A549 ACE2-/-C3、A549 ACE2-/-C6是两组敲除了ACE2基因的A549细胞,不清楚二者的区别。
12、SARS-CoV-2假病毒感染也依赖于HS(之前实验为蛋白-蛋白、蛋白-细胞结合实验,不是感染实验。感染是进入细胞,与细胞结合,即与细胞膜表面的受体结合只是感染的前奏),使用HSase预处理,使用外源性HS/heparin预处理,敲除EXT1、NDST1、HS6ST1/2都有效抑制了SARS-CoV-2假病毒对Vero
E6细胞(非洲绿猴肾细胞系细胞)的感染。如下图所示:
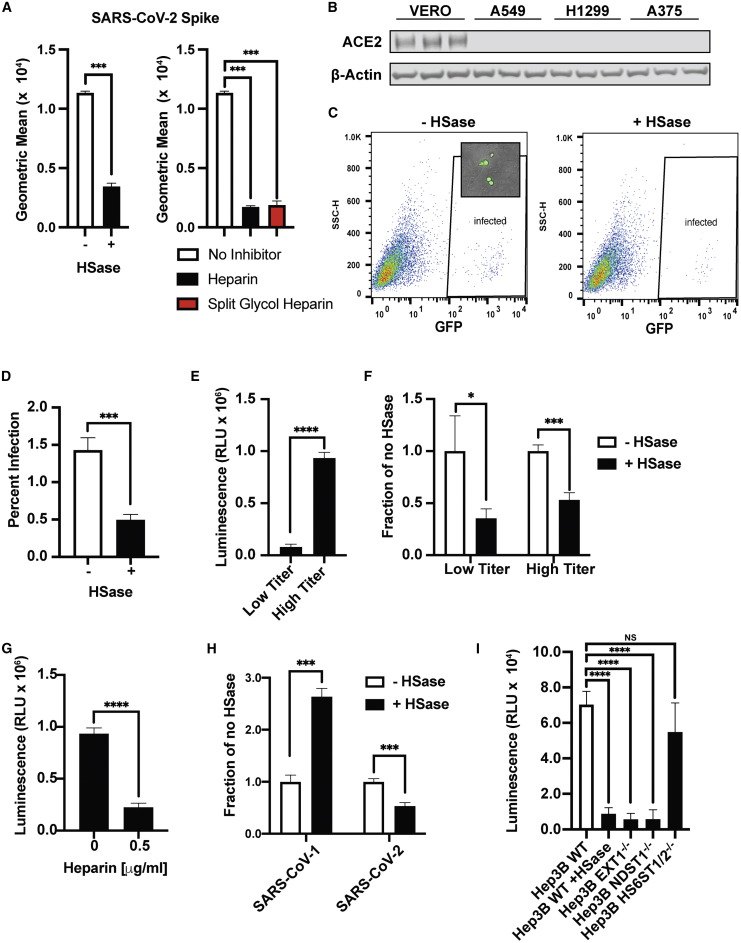
SARS-COV-2假病毒对Vero E6细胞的感染依赖于HS
SARS-CoV-2假病毒是用SARS-CoV-2 Spike蛋白替代VSV(vesicular stomatitis virus,水泡性口炎病毒)的G蛋白获得的;
13、如上图H所示,HSase(肝素裂解酶)显著抑制了SARS-CoV-2感染,但相比之下,HSase反而显著提升了SARS-CoV-1感染;与此同时,HSase对MERS-CoV感染也缺乏抑制作用,如下图所示:
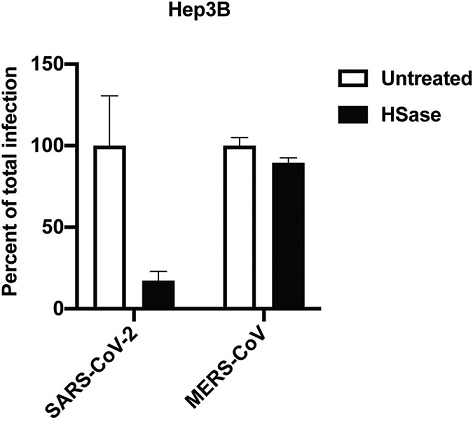
HSase不抑制MERS-CoV假病毒对Hep3B细胞的感染
可见,HS对SARS-COV-2感染的促进具有一定特异性;细胞膜表面的HS不是SARS-CoV-1和MERS-CoV的感染促进因子;HS可能干扰、抑制SARS-CoV-1的受体结合和细胞进入。
14、HS也是SARS-COV-2真病毒有效感染所需要的。
HSase、UFH预处理显著抑制了SARS-COV-2真病毒对Vero E6细胞的感染(下图B、C);
敲除NDST1完全抑制(消除)、敲除HS6ST1/2显著抑制了SARS-COV-2真病毒对Hep3B细胞的感染(下图D);
HSase、UFH预处理还显著(5倍以上)抑制了SARS-COV-2真病毒对原代人支气管上皮细胞(primary human bronchial epithelial cells)的感染(下图F、G)。
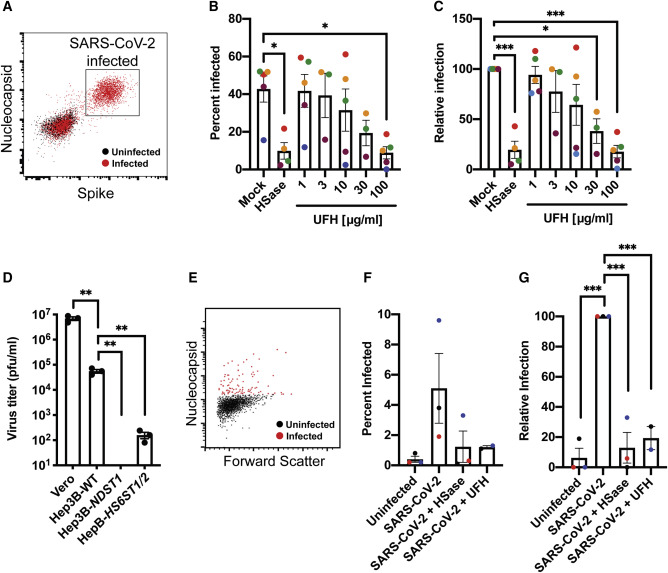
UFH:unfractionated heparin,未裂解肝素,也叫普通肝素,与UFH相对的是低分子量肝素。
论文依据二
Infection and transmission of SARS-CoV-2 depend on heparan sulfate proteoglycans
SARS-CoV-2的感染和传播依赖于硫酸乙酰肝素蛋白聚糖
https://www.embopress.org/doi/full/10.15252/embj.2020106765
论文要点如下:
1、确定了硫酸乙酰肝素蛋白聚糖(HSPG)是SARS-CoV-2的附着受体,且是ACE2受体的共受体。
2、UF heparin、anti-ACE2、及从COVID-19患者中分离出的三种SARS-CoV-2中和抗体都可干扰并显著抑制SARS-CoV-2假病毒与人类肝脏Huh7.5细胞的结合(图A);
用heparinase III去除细胞中的HS显著抑制了SARS-CoV-2假病毒与Huh7.5细胞的结合(图B);
敲除Exostosin-1(EXT1)基因及使用UF heparin极大抑制了SARS-CoV-2假病毒与Huh7.5细胞的结合(图D)。
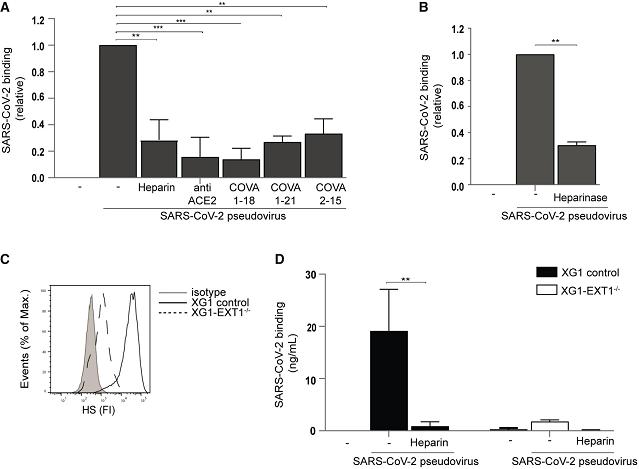
UF heparin,就是Unfractionated heparin(UFH),未裂解肝素或普通肝素。如前所述,heparin可结合、消耗SARS-2的S蛋白,干扰、抑制其与细胞表面HS/HSPG受体的结合。
anti-ACE2,ACE2中和抗体;
三种SARS-CoV-2中和抗体是两种RBD中和抗体COVA1-18、COVA2-15,及一种非RBD中和抗体COVA1-21;
heparinase III,肝素酶Ⅲ,一种多糖裂解酶,可切割、降解HS;
SARS-CoV-2假病毒是用SARS-CoV-2 S蛋白与去病毒性HIV-1骨架嵌合制作的;
Huh7是一种人类肝癌细胞系,Huh7.5 是Huh7的衍生细胞系;
如前所述,Exostosin-1(EXT1)是合成HS主链所需的一种糖基转移酶基因;
XG1/XG-1是一种人多发性骨髓瘤细胞,XG1-EXT1−/−是敲除了Exostosin-1(EXT1)基因的XG1细胞。
3、用四种(外源性添加的)LMWH(低分子量肝素)预处理细胞培养物显著抑制了SARS-CoV-2假病毒对Huh7.5细胞的结合、感染,它们的抑制效果与UF heparin(普通肝素)相当(下图A、图B、图C)。
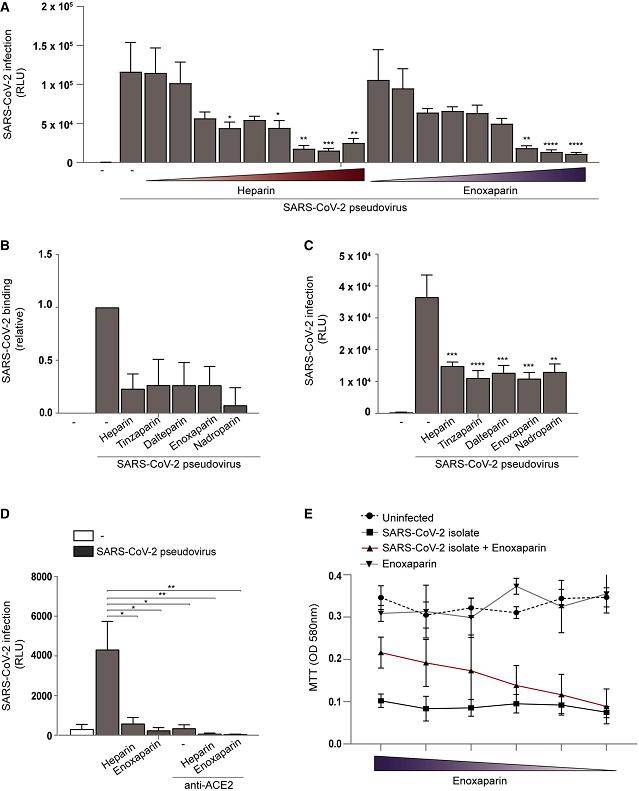
图A:UF heparin、enoxaparin抑制SARS-2假病毒对Huh7.5细胞的感染,抑制程度与浓度正相关;
图B:UF heparin、四种LMWH显著抑制SARS-2假病毒与Huh7.5细胞的结合;
图C:UF heparin、四种LMWH显著抑制SARS-2假病毒对Huh7.5细胞的感染;
图D:UF heparin、enoxaparin、anti-ACE2极大抑制了SARS-COV-2假病毒对293T-ACE2细胞的感染;
图E:说明略。
LMWH,low
molecular weight heparins,低分子量肝素,是普通肝素的人工裂解产物。LMWH、UF
heparin(UFH,未裂解肝素、普通肝素)是常用的抗凝血蛋白(抗凝血剂/抗血栓剂)。这二类肝素在本论文中都用作HS/HSPG干扰、抑制剂。
该研究使用了四种LMWH:tinzaparin、dalteparin 、enoxaparin、nadroparin,其中优先使用的是enoxaparin。
4、ACE2抗体显著抑制了SARS-CoV-2假病毒与Huh7.5细胞的结合(如前面要点2下的附图A所示);
ACE2抗体、UF heparin、enoxaparin都极大抑制了SARS-CoV-2假病毒对293T-ACE2细胞的感染(上图D)。
这两组结果表明,ACE2介导的SARS-CoV-2感染需要HS/HSPG,而HS/HSPG参与的SARS-CoV-2感染也需要ACE2,因此,HS/HSPG在SARS-CoV-2感染中是ACE2的共受体。
293T细胞即HEK293T细胞,是HEK293(Human Embryonic Kidney Cells 293,人胚胎肾细胞293)的衍生细胞系。293T-ACE2细胞是转染过表达ACE2的293T细胞,293T细胞自身应该不表达或极少表达ACE2。
5、UF heparin和LMWH(enoxaparin)有效抑制了SARS-COV-2假病毒、真病毒对两种极化状态的上皮细胞Caco-2(下图C)和Calu-3(下图D)的感染。
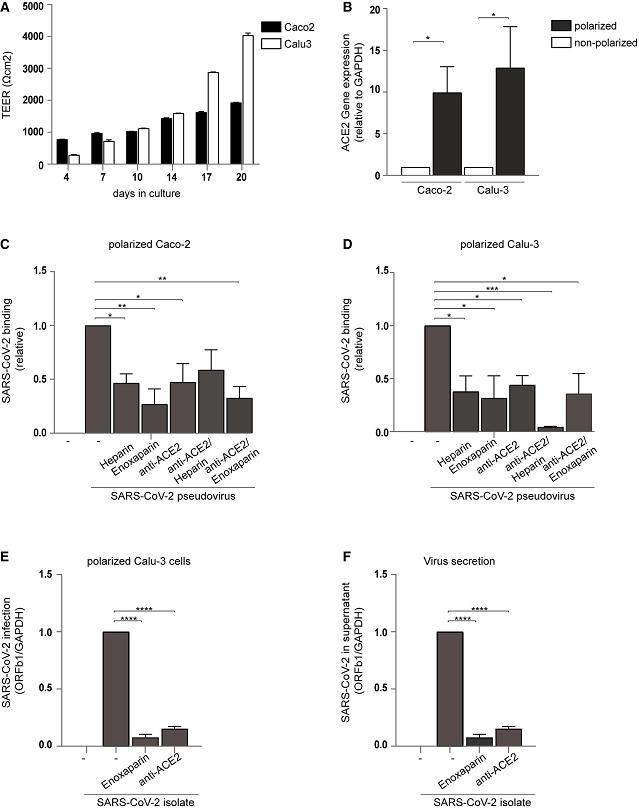
UF heparin、LMWH抑制SARS-2假病毒对极化的上皮细胞Caco-2、Calu-3的感染
图C:UF heparin、enoxaparin、anti-ACE2抑制SARS-2假病毒与Caco-2细胞的结合;
图D:UF heparin、enoxaparin、anti-ACE2抑制SARS-2假病毒与Calu-3细胞的结合;
图E、图F:enoxaparin、anti-ACE2抑制SARS-CoV-2真病毒对Calu-3细胞的感染。
图E对应(PCR测得的)成功感染的SARS-CoV-2相对计数;图F对应(PCR测得的)感染后复制产生并分泌到上清液(supernatant)中的SARS-CoV-2相对计数。
Caco-2是一种结直肠腺癌细胞系;
Calu-3是一种支气管腺癌细胞系;
SARS-CoV-2 isolate是一个分离自Italy的毒株。
笔者对极化的细胞认识欠清晰、确切。细胞在安静(未受刺激)时,细胞膜两侧外正内负的带电状态称为膜的极化状态,极化的细胞可能指细胞膜处于极化状态的,带电状态外正内负的细胞,或膜内外电位达到某一数值的细胞。大多数高等生物体在未受刺激时维持带负电的内部环境。HS/HSPG的聚糖链带高负电荷,极化的细胞外部带正电荷,二者容易相互吸引、结合。上图B显示,极化状态的Caco-2、Calu-3细胞的ACE2表达远高于非极化状态的Caco-2、Calu-3细胞,不清楚造成这种突出差异的原因。
6、HSPG对SARS-CoV-2的细胞结合很重要。两种HSPG
Syndecan 1或Syndecan 4的转染表达显著提升了SARS-CoV-2假病毒、真病毒与Namalwa细胞的结合;外源性UF
heparin和LMWH(enoxaparin)均显著抑制了SARS-CoV-2假病毒、真病毒与Namalwa细胞的结合。如下图所示:
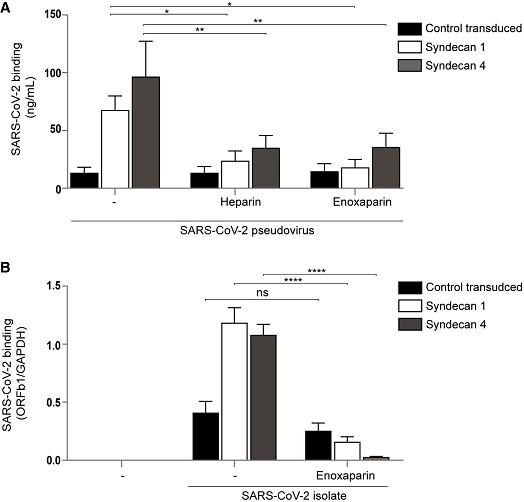
图A:Syndecan 1或Syndecan 4的转染表达显著提升了SARS-2假病毒与Namalwa细胞的结合;UF heparin、enoxaparin显著抑制了SARS-2假病毒与Namalwa细胞的结合。
图B:Syndecan 1或Syndecan 4的转染表达显著提升了SARS-2真病毒与Namalwa细胞的结合;enoxaparin显著抑制了SARS-2真病毒与Namalwa细胞的结合。
Namalwa是一种人淋巴瘤细胞系,Namalwa细胞本身既不表达HS/HSPG,也不表达ACE2。SARS-2可结合转染表达HSPG的Namalwa细胞(与细胞表面的HSPG结合),但未造成感染(未进入细胞)。
7、三种SARS-CoV-2中和抗体COVA1-18、COVA2-15、COVA1-21有效抑制了SARS-CoV-2与转染表达Syndecan
1的Namalwa细胞的结合,三种抗体的抑制效果与enoxaparin相当。一些SARS-CoV-2的非中和抗体没有相应的抑制作用。如下图所示:
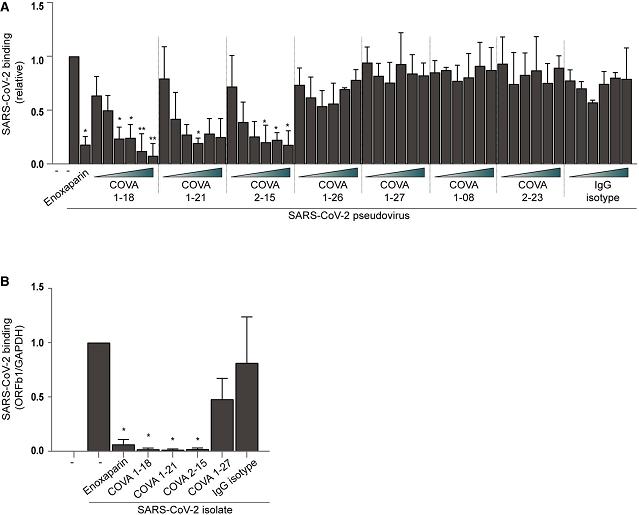
图A:COVA1-18、COVA2-15、COVA1-21、enoxaparin有效抑制了SARS-2假病毒与Syndecan 1-Namalwa细胞的结合;
图B:COVA1-18、COVA2-15、COVA1-21、enoxaparin有效抑制了SARS-2真病毒与Syndecan 1-Namalwa细胞的结合。
这些结果再次表明,SARS-2通过S蛋白结合HSPG,从而与细胞结合。
笔者注:三种SARS-2中和抗体的SARS-2-S RBD结合位点,与Syndecan 1或HSPG的SARS-2-S RBD结合位点应该存在重合、竞争。
8、不表达ACE2的树突状细胞(DC,Dendritic
Cells)和皮肤粘膜朗格汉斯细胞(LC,Langerhans
cells,DC细胞的一个子类)不会被SARS-CoV-2感染,但这两个DC亚群可通过HSPG(硫酸乙酰肝素蛋白聚糖)有效结合、捕获SARS-CoV-2,并将病毒传播给表达ACE2的人肝脏Huh7.5细胞,并导致Huh7.5细胞被感染。这(携带SARS-2的DC细胞的迁移)也可能是SARS-CoV-2从呼吸道粘膜到达、感染淋巴组织的传播途径。
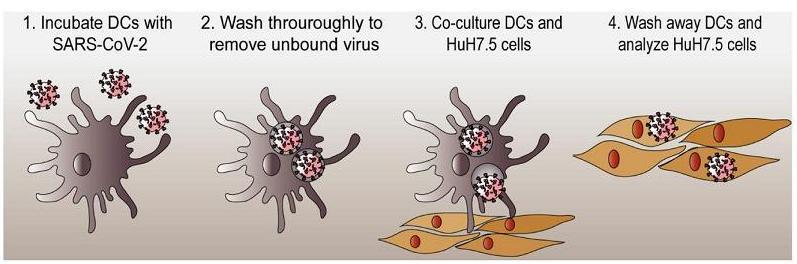
ACE2阴性的DC细胞结合、携带SARS-2并造成ACE2阳性的Huh7.5被感染
SARS-CoV-2的上述传播方式与DC细胞体内传播HIV-1相似。
9、LMWH(enoxaparin)可防止DC细胞亚群体内传播SARS-CoV-2。
10、SARS-CoV-2真病毒可结合、感染原代鼻细胞(primary nasal cells),使用enoxaparin可显著抑制结合与感染,这表明HSPG参与SARS-2对原代鼻细胞的感染。
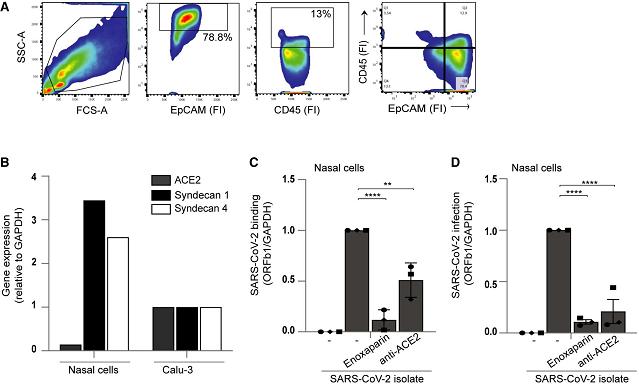
图B:原代鼻细胞高表达两种HSPG,同时有少量ACE2表达;
图C:SARS-2可结合原代鼻细胞,enoxaparin、anti-ACE2不同程度抑制二者的结合;
图D:SARS-2可感染原代鼻细胞,enoxaparin、anti-ACE2不同程度抑制SARS-2对原代鼻细胞的感染。
论文依据三
Heparan
Sulfate Facilitates Spike Protein-Mediated SARS-CoV-2 Host Cell
Invasion and Contributes to Increased Infection of SARS-CoV-2 G614
Mutant and in Lung Cancer
硫酸乙酰肝素促进刺突蛋白介导的SARS-CoV-2宿主细胞侵袭,并增加了SARS-CoV-2 G614突变体和肺癌(患者)的感染
https://www.frontiersin.org/articles/10.3389/fmolb.2021.649575/full
论文指出:
1、硫酸乙酰肝素(HS)可以结合SARS-CoV-2刺突蛋白(S蛋白),并在细胞表面与ACE2协同介导SARS-CoV-2对宿主细胞的感染;
2、宿主细胞表面(应指细胞膜)与SARS-2-S的结合取决于宿主细胞表面的HS表达,这种结合是SARS-CoV-2感染宿主细胞所必需的;
3、SARS-CoV-2 S蛋白与细胞的结合可以被肝素裂解酶HSase、HS拮抗剂surfen、肝素(heparin,HP)和多种肝素衍生物阻断;
4、肝素/HS与SARS-2-S的结合主要由它们的整体硫酸化决定,特定SARS-2-S结合基序对结合的潜在贡献较小;
5、SARS-2-S G614突变体与肝素的较高结合亲和力和上调的HS表达,可能是SARS-CoV-2 G614突变体具有较高传染性,和肺癌患者对SARS-CoV-2感染高度易感的部分原因;
6、SARS-CoV-2 G614变体假病毒对宿主细胞的较高感染以及HS表达上调引起的感染增强可被肝素裂解酶HSase和肝素有效阻断,也可能被surfen和肝素衍生物阻断;
7、我们的研究结果支持,阻断HS与SARS-2-S的相互作用可能有助于COVID-19的预防和治疗。
SARS-CoV-2
G614突变体即D614G突变体,其S蛋白第614氨基酸由天冬氨酸D突变为甘氨酸G。G614突变体感染能力更强,传播更快,其感染滴度相比D614毒株增加2.6至9.3倍。G614突变体2020年1月底在中国和德国收集的病毒中开始被检测到,2020年5月前后,G614突变体成为全球主导性的SARS-CoV-2
毒株。
其它论文依据或相关论文
Heparan sulfate assists SARS-CoV-2 in cell entry and can be targeted by approved drugs in vitro
硫酸乙酰肝素协助SARS-CoV-2进入细胞,并可被批准的体外药物靶向
https://www.nature.com/articles/s41421-020-00222-5
Host and viral determinants for efficient SARS-CoV-2 infection of the human lung
SARS-CoV-2有效感染人肺的宿主和病毒决定因素
https://www.nature.com/articles/s41467-020-20457-w
Heparan Sulfate Proteoglycans in Viral Infection and Treatment: A Special Focus on SARS-CoV-2
病毒感染和治疗中的硫酸乙酰肝素蛋白多糖(HSPGs):对SARS-CoV-2的特别关注
https://www.mdpi.com/1422-0067/22/12/6574
Characterization
of heparin and severe acute respiratory syndrome-related coronavirus 2
(SARS-CoV-2) spike glycoprotein binding interactions
肝素和严重急性呼吸综合征相关冠状病毒2(SARS-CoV-2)刺突糖蛋白结合相互作用的表征
https://pubmed.ncbi.nlm.nih.gov/32653452/
6、Vimentin(VIM)
Vimentin(VIM),波形蛋白,也叫波形纤维蛋白,是一种III型中间丝蛋白质(Intermediate Filament Protein)。
中间丝蛋白是真核生物细胞的重要结构蛋白,中间丝蛋白、微管蛋白、肌动蛋白微细丝,三者合称细胞骨架(蛋白)。
波形蛋白是间质细胞骨架的主要组成部分。波形蛋白围绕细胞核并跨越细胞外围,在细胞内形成动态且灵活的网络,维持细胞的结构、形态、完整性,并在多种细胞事件中发挥重要作用。
波形蛋白(Vimentin)形态示意图
Vimentin(VIM)是细胞分化过程中最先表达的蛋白。VIM在成纤维细胞(结缔组织中最常见的细胞)、内皮细胞、平滑肌细胞、黑色素细胞、雪旺细胞(Schwann
cell,神经胶质细胞、神经膜细胞)、多种免疫系统细胞(巨噬细胞、单核细胞、粒细胞以及T和B淋巴细胞)等等间充质来源的细胞及软组织中广泛表达,Vimentin也在肺泡II型细胞和鼻杯状分泌细胞中表达,vimentin还在多种肿瘤组织中高表达,并与肿瘤的发生、发展和侵袭转移密切相关。
波形蛋白(Vimentin,VIM)主要位于细胞质中,它也出现在细胞膜表面和细胞外介质中,在一些细胞(如II型肺泡细胞和鼻腔分泌细胞)表面,波形蛋白有很高的表达。
细胞表面的波形蛋白是多种病菌、病毒感染细胞所需的受体、共受体或附着因子,这些病原体包括Escherichia
coli K1(大肠杆菌K1,新生儿脑膜炎的病原体)、Streptococcus pyogenes(化脓性链球菌)、enterovirus
71(肠道病毒71型)、dengue virus(登革热病毒)、cowpea mosaic
virus(豇豆花叶病毒,一种植物病毒)、Japanese encephalitis virus (日本脑炎病毒)、human
papillomavirus(HPV,人乳头瘤病毒,尖锐湿疣的病原体)、SARS-CoV等,其中,vimentin是SARS-CoV-1的主要受体ACE2的共受体(辅助受体)。
类似SARS-CoV-1,vimentin也是SARS-CoV-2的重要受体ACE2的共受体(辅助受体)。
论文依据一
Vimentin is an important ACE2 co-receptor for SARS-CoV-2 in epithelial cells
波形蛋白是SARS-CoV-2在上皮细胞中的一种重要ACE2共受体
https://www.cell.com/iscience/fulltext/S2589-0042(22)01735-7
https://www.sciencedirect.com/science/article/pii/S2589004222017357
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9618295/
论文指出:
1、SARS-COV-2感染上调波形蛋白在细胞表面的表达。
2、SARS-COV-2对A549细胞的感染能力微弱,相比表达ACE2的Vero
E6细胞和Caco-2细胞,A549细胞中的SARS-COV-2拷贝数低300倍。A549细胞高水平表达波形蛋白,但不表达ACE2。这表明波形蛋白不能独立介导SARS-COV-2感染。
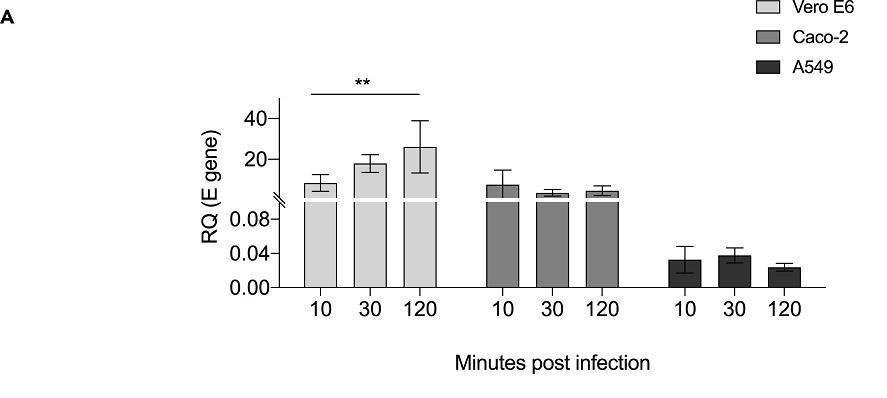
SARS-COV-2对Vero E6、Caco-2、A549细胞的感染能力
提醒列位注意,纵坐标的上下两段不是等比例的,条柱高度比不代表感染能力比。
RQ:Relative Quantity,相对数量;
RQ(E gene):(感染进入细胞中的)SARS-COV-2 E蛋白基因的(qPCR检测)相对数量。E蛋白即包膜蛋白(envelope)。
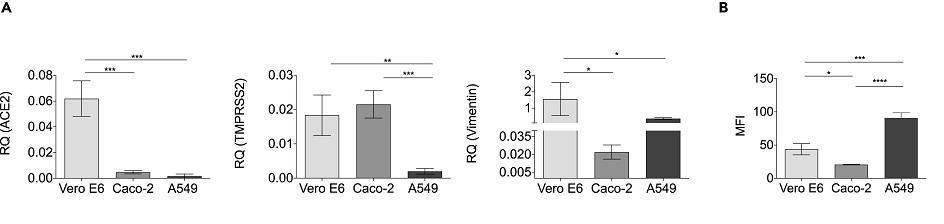
图A:通过qPCR检测ACE2、TMPRSS2、vimentin在三种细胞中的表达丰度;
图B:通过流式细胞术评估细胞外表vimentin的表达丰度,并表示为平均荧光强度(MFI)。
MFI:mean fluorescence intensity,平均荧光强度。
3、SARS-COV-2
S蛋白、波形蛋白、ACE2在上皮细胞(Vero
E6细胞)表面相互作用,形成三分子复合物,SARS-COV-2通过三者的相互作用进入细胞。当细胞未被感染时,观察不到波形蛋白与ACE2之间的相互作用(VIM-ACE2的相互作用与SARS-2感染挂钩)。2、3表明,波形蛋白是SARS-COV-2的重要受体ACE2的共受体(辅助受体)。
4、细胞表面波形蛋白的存在有利于SARS-COV-2感染。SARS-CoV-2对Caco-2细胞的感染效率低于Vero E6细胞(见前图)。Caco-2细胞高表达ACE2但几乎不表达波形蛋白,而Vero E6细胞同时高表达ACE2和波形蛋白(见上图)。
5、抑制细胞表面的波形蛋白降低了SARS-COV-2的细胞进入和细胞毒性。
a)用波形蛋白结合、干扰、重组剂withaferin A(WFA)或抗波形蛋白V9单克隆抗体预处理Vero E6细胞,都可使SARS-COV-2感染减少50%以上。
withaferin A(WFA,醉茄素A)是一种类固醇内酯,能够结合波形蛋白,扰乱其表达,并诱导波形蛋白在细胞核周围重组为核周聚集体。
b)相比未经处理的Vero E6细胞,用WFA或V9抗体预处理Vero E6细胞提高了细胞感染后48小时的活力,这表明抑制波形蛋白可以抑制SARS-COV-2的细胞毒性,减少或减缓细胞死亡。
6、波形蛋白与SARS-COV-2的相互作用调节炎性细胞因子和趋化因子的表达,抗波形蛋白V9单克隆抗体预处理导致IL-6表达下降15倍,CCL5和CXCL10表达下降10倍,这些数据表明波形蛋白参与(、影响)SARS-CoV-2介导的细胞死亡和上皮炎症反应。
IL-6,一种多效细胞因子,细胞因子风暴的诱因;
CCL5,一种趋化因子,诱发白细胞/免疫细胞附着及转移至发炎部位;
CXCL10,一种趋化因子,是活化的T淋巴细胞、单核细胞、巨噬细胞、自然杀伤细胞等白细胞/免疫细胞的化学引诱剂,可趋化上述细胞到达炎症部位,发挥抗炎免疫作用。CXCL10基因也是一种血管抑制因子。
7、实验表明,波形蛋白与SARS-CoV-2原始毒株S蛋白的相互作用,对原始毒株感染的促进在omicron变体中得到了保持,即omicron变体S蛋白的一系列突变没有改变波形蛋白与SARS-CoV-2
S蛋白的相互作用,没有改变波形蛋白对SARS-CoV-2感染能力的促进作用。
8、总之,我们的数据表明,在SARS-COV-2感染中,细胞表面波形蛋白是ACE2的共受体。
论文依据二
Extracellular vimentin is an attachment factor that facilitates SARS-CoV-2 entry into human endothelial cells
细胞外波形蛋白是促进SARS-COV-2进入人内皮细胞的附着因子
https://www.pnas.org/doi/10.1073/pnas.2113874119
论文指出:
1、使用液相色谱-串联质谱法(LC-MS/MS),鉴定出vimentin(VIM)是一种与SARS-CoV-2
S蛋白结合的蛋白质,S蛋白通过其受体结合域(RBD)与细胞外表的VIM相互作用、结合;VIM在SARS-COV-2感染中充当ACE2的共受体(辅助受体)。
2、SARS-CoV-2对HEK-293细胞的感染能力微弱。HEK-293细胞既不表达ACE2,也不表达VIM(波形蛋白);
对转染表达VIM的HEK-293细胞,SARS-CoV-2的感染能力没有明显提升;
对转染表达ACE2的HEK-293细胞,SARS-CoV-2的感染能力显著提升;
对同时转染ACE2和VIM的HEK-293细胞,SARS-CoV-2的感染能力进一步提升。
如下图B所示:
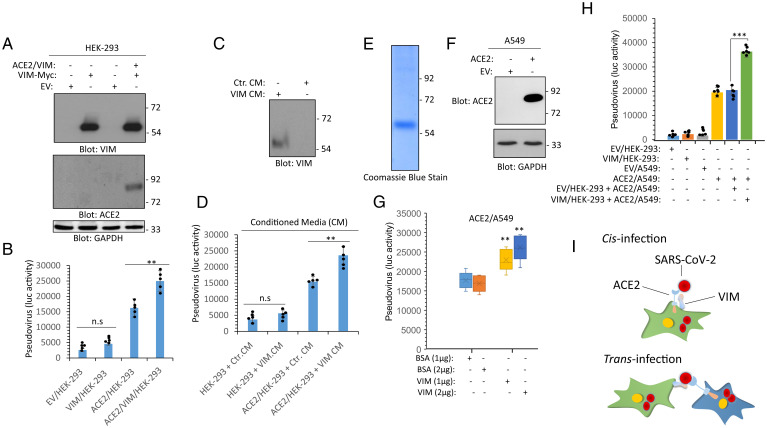
可见,VIM与ACE2的共表达促进SARS-CoV-2对HEK-293细胞的感染,VIM对SARS-CoV-2感染的促进依赖于ACE2的存在。
该组感染实验所用病毒为以SARS-CoV-2 S蛋白嵌合制作的假病毒。
3、VIM、ACE2的跨细胞表达也能显著提升SARS-CoV-2的感染。将VIM/HEK-293细胞(转染表达VIM的HEK-293细胞)与ACE2/A549细胞(转染表达ACE2的A549
细胞)共培养显著提升了SARS-CoV-2对ACE2/A549 细胞的感染。如上图H所示。
4、VIM可同时与SARS-COV-2 S和ACE2相互作用;VIM与ACE2的相互作用提升了SARS-COV-2 S与ACE2的结合效率,并使结合更牢固;SARS-2 S-RBD的VIM结合位点,与S-RBD的ACE2结合位点不同。
5、一种SARS中和抗体CR3022可识别、结合SARS-CoV-2-S-RBD中的独特表位(如下图A所示),CR3022抗体不干扰、抑制S与ACE2的结合,但干扰、抑制SARS-2
S-RBD与VIM的结合。这表明,SARS-2
S-RBD结合VIM的部位,与其结合CR3022抗体的部位存在重合。CR3022抗体是从SARS患者恢复期血浆中鉴定出来的。
6、CR3022抗体抑制SARS-CoV-2对HUVEC-TERT细胞的感染,但当HUVEC-TERT细胞敲低了VIM表达时,CR3022对SARS-2感染没有明显的抑制作用。即CR3022抗体对SARS-CoV-2感染的抑制仅对充分表达VIM的细胞有效(CR3022实质上是在干扰、抑制SARS-2
S与VIM的结合)。如下图F所示:
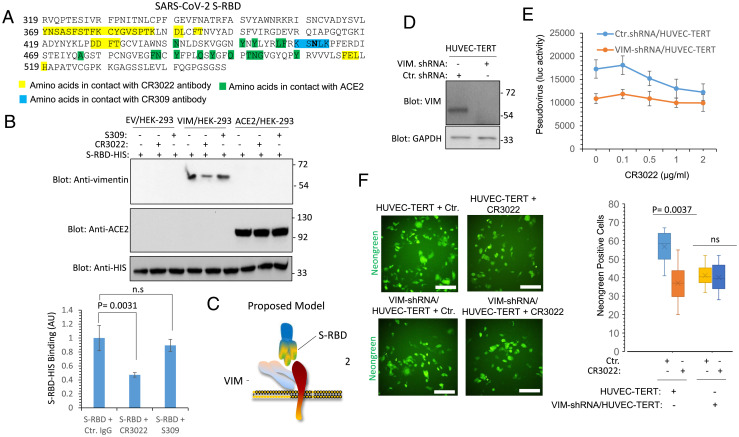
HUVEC-TERT:human umbilical vein endothelial cells,人脐静脉内皮细胞;
VIM-shRNA/HUVEC-TERT:通过shRNA敲低了VIM表达的HUVEC-TERT细胞;
shRNA:hort-hairpin RNA,短发夹RNA ,可用于基因沉默,干扰、抑制特定基因。
7、相关实验进一步表明,SARS-CoV-2对共表达VIM 和ACE2的HEK-293细胞的感染率明显高于仅表达ACE2的细胞(下图A);敲低VIM显著抑制了SARS-CoV-2对HUVEC-TERT细胞的感染(下图B)。
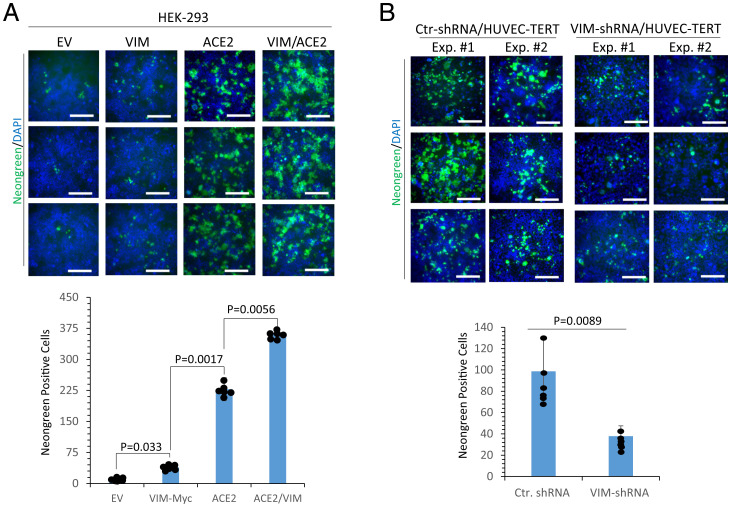
8、内皮细胞是SARS-CoV-2的直接感染靶标,内皮细胞感染以及SARS-CoV-2诱导的炎症反应可导致多种症状(其中两种是血管生成改变和神经系统症状)。SARS-CoV-2诱导的内皮损伤、血管血栓形成和凝血病,以及冯维勒布兰德因子上调,都是严重COVID-19的临床标志。
9 、总之,VIM是SARS-CoV-2的附着因子和辅助受体,可增强ACE2依赖性病毒进入,在SARS-CoV-2感染人内皮细胞中发挥重要作用。
论文依据三
Extracellular Vimentin as a Target Against SARS-CoV-2 Host Cell Invasion
细胞外波形蛋白是SARS-COV-2侵袭宿主细胞的靶标
https://onlinelibrary.wiley.com/doi/full/10.1002/smll.202105640
论文指出:
1、动态光散射显示波形蛋白与带有SARS-CoV-2 S蛋白的假病毒结合;
2、针对波形蛋白的抗体可在体外阻断SARS-CoV-2假病毒对表达ACE2的细胞的感染;
3、1、2表明细胞外波形蛋白是SARS-CoV-2的受体ACE2的共同受体;
4、SARS-CoV-2 S蛋白与波形蛋白的结合亲和力小于S蛋白与ACE2的结合亲和力;
5、细胞外波形蛋白可能作为SARS-CoV-2 S蛋白-ACE2复合物的关键成分,介导SARS-CoV-2进入细胞;
6、波形蛋白靶向药物可能预防和减缓SARS-CoV-2感染。
论文依据四
Physicochemical Nature of SARS-CoV-2 Spike Protein Binding to Human Vimentin
SARS-COV-2刺突蛋白与人类波形蛋白结合的物理化学性质
https://pubs.acs.org/doi/10.1021/acsami.3c03347
论文“Conclusions”部分译文大致如下:
使用AFM(atomic
force microscopy,原子力显微镜)和QCM-D(quartz crystal microbalance with energy
dissipation,具有能量耗散的石英晶体微天平)方法,对SARS-CoV-2原始毒株和三种变体(巴西、南非和英国)的S1
RBD与Vim之间相互作用的生物力学和动力学进行了研究,为S1
RBD与Vim相互作用的机械强度和稳定性提供了新的证据。证实了先前生物学研究的结果,即确定Vim是病毒进入宿主细胞的可能附着面。此外,还对SARS-CoV-2–ACE2与Vim二聚体之间的假定相互作用场景进行了原位探索,验证了Vim-S1
RBD与ACE2-S1
RBD之间可能的接触残基。我们的研究结果将有助于充分了解病毒进入宿主细胞的机制、开发安全有效的预防以及治疗Covid-19的新方法。Vim和病毒融合蛋白之间的界面相互作用研究还可用于开发新的功能性抗病毒材料或生产模拟SARS-CoV-2病毒颗粒的纳米粒子,用于(便利的)实验室的生物研究,无需达到处理天然SARS-CoV-2毒株所需的生物安全级别3,考虑到SARS-CoV-2病毒和后续突变引起的疾病在未来几年将继续成为医学领域的主要挑战之一,这一点尤为重要。
其它相关论文
Vimentin as a target for the treatment of COVID-19
波形蛋白作为COVID-19治疗的靶点
https://bmjopenrespres.bmj.com/content/7/1/e000623
Extracellular
vimentin is sufficient to promote cell attachment, spreading, and
motility by a mechanism involving N-acetyl glucosamine-containing
structures
细胞外波形蛋白足以通过与含N-乙酰葡萄糖胺结构相关的机制来促进细胞附着,扩散和运动
https://www.jbc.org/article/S0021-9258(23)01991-9/fulltext
(未完待续)
|
