

2020-02-17 12:39:13


     



     
用了十五年时间寻找蝙蝠,又花费了数年研究蝙蝠基因、发表学术论文,完成对SARS(非典)宿主蝙蝠的溯源,石正丽有“蝙蝠女侠”之称。 在新冠肺炎疫情肆虐下,因为一则简短的声明,石正丽火了。 2月2日,石正丽表示“用生命担保”新冠肺炎病毒(SARS-CoV)与武汉病毒所没有关系,并要求那些相信人造病毒泄露的人“闭上臭嘴”。 
 2020年2月16日,又因为新冠肺炎“零号病人”黄燕玲传闻,石正丽出来担保称武汉病毒所没人感染,零号传染源与武汉病毒所无关。 2020年2月16日,又因为新冠肺炎“零号病人”黄燕玲传闻,石正丽出来担保称武汉病毒所没人感染,零号传染源与武汉病毒所无关。
石正丽屡屡成为当前有关新冠肺炎的舆论风口浪尖的人物,是有原因的。社会对她持续的关注在于,她掌握了大量的蝙蝠体内的病毒及其基因组信息,且参与过人造病毒重组实验。见:石正丽,科学狂人与科学伦理  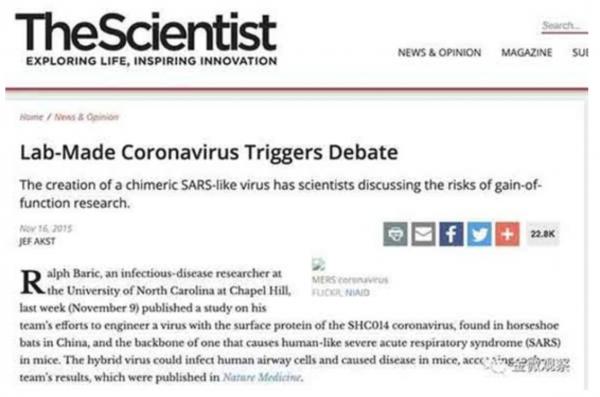
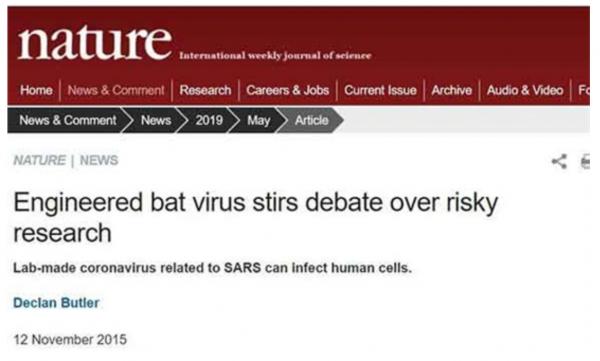 美国科学家和自然的报道 美国科学家和自然的报道
关于人造病毒的试验,2015年国际著名期刊《Nature Medicine(自然医学)》的一篇论文《一个类似SARS的蝙蝠冠状病毒群显示了人类出现的可能性》,记载了这一切。这项发现美国《科学家》对此作了报道,使用SARS冠状病毒骨架和来自中华菊头蝠的SHC014冠状病毒表面蛋白进行工程化改造,在实验室创造了一种杂交冠状病毒,这一冠状病毒可以感染人的呼吸道细胞,并能引起小鼠疾病。后来,又有美国医学专家在美国《自然》上撰文,批评这种实验存在一定的道德和安全风险。 
这是论文摘要的翻译: 严重急性呼吸综合征冠状病毒(SARS-CoV)和中东呼吸综合征(MERS)-CoV的出现突出了跨物种传播事件导致人类暴发的威胁。在这里,我们研究了目前在中国马蹄蝠种群中传播的SARS样CoVs的疾病潜力。利用SARS-CoV反向遗传系统,我们产生了一种嵌合病毒,该病毒在小鼠适应SARS-CoV的主干中表达了蝙蝠冠状病毒SHC014的峰值。结果表明,由2b组的野生型基础中的突变而来SHC014编码的病毒,可以高效利用SARS受体人血管紧张素转换酶II (ACE2)的多个同源体。其能够在人呼吸道分离的原代细胞中高效地复制,并在体外能够达到与SARS-CoV流行株等值的病毒滴度。此外,体内实验证明嵌合病毒在小鼠肺部的复制具有明显的发病机制。对现有基于SARS的免疫治疗和预防模式的评估显示效果不佳;单克隆抗体和疫苗方法,未能利用这种新的S蛋白中和,并不能保护细胞免于冠状病毒的感染。基于这些发现,我们合成了一种具有感染性的全长SHC014重组病毒,并在体内外展示了病毒的强大复制能力。我们的工作表明,目前在蝙蝠种群中传播的病毒有重新出现SARS-CoV的潜在风险。 SARS病毒的模型,紫色为S蛋白 关于这个实验的大意:利用病毒基因重组技术将蝙蝠体内的RsSHC014-CoV和HIV病毒重组成人造病毒SHC014,得到的人造病毒可以和人体细胞上的血管紧张素转化酶2(ACE2)结合,能很有效地感染人类的呼吸道细胞,毒性巨大。试验重组的人造病毒SHC014明显地损害了实验小鼠的肺部,参与实验的所有疫苗对人造病毒失去中和作用。这个实验最关键的部分是:科研团队把一个本来对人没有侵染性的蝙蝠体内病毒RsSHC014-CoV,通过插入对人体细胞ACE2受体有亲和力的基因片段而让人造病毒SHC014变成了对人类传染性的病毒。那是因为细胞上对SARS-CoV有亲和力的ACE2受体被利用了,相当于用基因重组技术成功构建了一个新的对人体细胞有侵染性毒性的冠状病毒。 
 很多人会说,这是一个团队的集体成果,石正丽在其中扮演了什么角色。关于论文作者的贡献,石正丽是位于作者的第9位,贡献是:Z.-L.S. provided SHC014 spike sequences and plasmids。翻译为:石正丽提供了SHC014S蛋白基因序列和质粒。 很多人会说,这是一个团队的集体成果,石正丽在其中扮演了什么角色。关于论文作者的贡献,石正丽是位于作者的第9位,贡献是:Z.-L.S. provided SHC014 spike sequences and plasmids。翻译为:石正丽提供了SHC014S蛋白基因序列和质粒。
无论是论文摘要还是论文全文,都有关于人造病毒SHC014的介绍,体现了这个病毒的重要性。由于多年来石正丽研究团队持续不断地寻找蝙蝠,让该团队掌握有大量的病毒基因数据,包括了马蹄蝠体内的冠状病毒基因数据,这就相当于构建人造病毒的基础原材料。 
 关于这个实验,论文的遗传系谱图显示:试验是用蝙蝠中的冠状病毒RsSHC014和HIV病毒来重组的人造病毒SHC014。论文中提到,假分型实验与使用HIV为基础的假病毒的实验相似,制备方法如前所述,并在表达ACE2原基的Hela细胞(武汉病毒所)上进行检测。 关于这个实验,论文的遗传系谱图显示:试验是用蝙蝠中的冠状病毒RsSHC014和HIV病毒来重组的人造病毒SHC014。论文中提到,假分型实验与使用HIV为基础的假病毒的实验相似,制备方法如前所述,并在表达ACE2原基的Hela细胞(武汉病毒所)上进行检测。
论文主要作者有八个,其中大部分是国外作者,这些作者的分工大致是:VDM设计、协调、实验执行、分析完成、稿件撰写。布莱设计了传染性克隆体并回收了嵌合病毒。SA完成中和试验。LEG帮助进行小鼠实验,TS和JAP完成小鼠实验和斑块检测。XG进行了伪分型实验。KD生成了结构数据和预测。ED生成系统发育分析。RLG完成RNA分析。SHR提供了人呼吸道上皮原代培养物。AL和WM提供了关键的单克隆抗体试剂。ZLS提供了SHC014的S蛋白基因序列和质粒。RSB设计实验并撰写手稿。 论文最后写到,研究得到了美国国立科学研究院的资助,过敏和传染病与美国国家老龄化研究所卫生研究院(NIH)、还有生态健康联盟(ZLS)、北卡罗来纳大学等支持。 那么问题来了: 1、石正丽从基础性的材料——马蹄蝠中,分离出了冠状病毒RsSHC014,与HIV病毒来重组,最终试验完成了人造病毒SHC014。石正丽做了哪些工作? 2、这个实验中,有大量的国外作者,其中有些老外负责设计实验,有些负责克隆实验,有些负责小鼠实验等,而这些实验多是在国外作的,也就是说,美国人做的侵染性实验和毒理实验,这些需要原料。这两个步骤如何走到一起的? 3、中外合作性实验,不同的步骤组合,需要在线下完成,只有两种可能结果:要么老外们集体来中国做后续实验,要么石正丽提供原材料出境一起作实验。如果SHC014人造病毒到国外的话,它们是如何到的美国?海关登记如何的? 4、石正丽参与此论文工作,是否经过所在单位的审查批准,包括科技伦理审查意见是什么?向外方提供基因材料是否需单位同意?在外方质疑该研究危险性之后,石所在单位和上级主管部门作何反应? 最后,我们尊重科学家的工作,但论文摆在眼前,人造病毒写在其中,石正丽贡献栏里写着提供“SHC014蛋白基因序列和质粒”,石扮演着重要角色。石正丽作为团队一员,对SHC014人造病毒应该非常清楚。这里,我只想问问石正丽,2015年那次合成的人造病毒去哪了? 2020年2月16日 https://www.kunlunce.com/ssjj/guojipinglun/2020-02-17/140607.html


Abstract
The emergence of severe acute respiratory syndrome coronavirus (SARS-CoV) and Middle East respiratory syndrome (MERS)-CoV underscores the threat of cross-species transmission events leading to outbreaks in humans. Here we examine the disease potential of a SARS-like virus, SHC014-CoV, which is currently circulating in Chinese horseshoe bat populations1. Using the SARS-CoV reverse genetics system2, we generated and characterized a chimeric virus expressing the spike of bat coronavirus SHC014 in a mouse-adapted SARS-CoV backbone. The results indicate that group 2b viruses encoding the SHC014 spike in a wild-type backbone can efficiently use multiple orthologs of the SARS receptor human angiotensin converting enzyme II (ACE2), replicate efficiently in primary human airway cells and achieve in vitro titers equivalent to epidemic strains of SARS-CoV. Additionally, in vivo experiments demonstrate replication of the chimeric virus in mouse lung with notable pathogenesis. Evaluation of available SARS-based immune-therapeutic and prophylactic modalities revealed poor efficacy; both monoclonal antibody and vaccine approaches failed to neutralize and protect from infection with CoVs using the novel spike protein. On the basis of these findings, we synthetically re-derived an infectious full-length SHC014 recombinant virus and demonstrate robust viral replication both in vitro and in vivo. Our work suggests a potential risk of SARS-CoV re-emergence from viruses currently circulating in bat populations.
MainThe emergence of SARS-CoV heralded a new era in the cross-species transmission of severe respiratory illness with globalization leading to rapid spread around the world and massive economic impact3,4. Since then, several strains—including influenza A strains H5N1, H1N1 and H7N9 and MERS-CoV—have emerged from animal populations, causing considerable disease, mortality and economic hardship for the afflicted regions5. Although public health measures were able to stop the SARS-CoV outbreak4, recent metagenomics studies have identified sequences of closely related SARS-like viruses circulating in Chinese bat populations that may pose a future threat1,6. However, sequence data alone provides minimal insights to identify and prepare for future prepandemic viruses. Therefore, to examine the emergence potential (that is, the potential to infect humans) of circulating bat CoVs, we built a chimeric virus encoding a novel, zoonotic CoV spike protein—from the RsSHC014-CoV sequence that was isolated from Chinese horseshoe bats1—in the context of the SARS-CoV mouse-adapted backbone. The hybrid virus allowed us to evaluate the ability of the novel spike protein to cause disease independently of other necessary adaptive mutations in its natural backbone. Using this approach, we characterized CoV infection mediated by the SHC014 spike protein in primary human airway cells and in vivo, and tested the efficacy of available immune therapeutics against SHC014-CoV. Together, the strategy translates metagenomics data to help predict and prepare for future emergent viruses.
抽象的严重急性呼吸综合征冠状病毒 (SARS-CoV) 和中东呼吸综合征 (MERS)-CoV 的出现凸显了导致人类爆发的跨物种传播事件的威胁。在这里,我们研究了一种 SARS 样病毒 SHC014-CoV 的疾病潜力,该病毒目前在中国马蹄蝠种群1 中传播。使用 SARS-CoV 反向遗传学系统2,我们生成并表征了一种嵌合病毒,该病毒在小鼠适应的 SARS-CoV 骨架中表达蝙蝠冠状病毒 SHC014 的尖峰。结果表明,在野生型骨架中编码 SHC014 尖峰的 2b 组病毒可以有效地使用 SARS 受体人血管紧张素转化酶 II (ACE2) 的多个直向同源物,在原代人气道细胞中有效复制,并实现与流行病相当的体外滴度SARS-CoV 病毒株。此外,体内实验证明嵌合病毒在小鼠肺中的复制具有显着的发病机制。对现有的基于 SARS 的免疫治疗和预防方法的评估显示疗效不佳;使用新型刺突蛋白,单克隆抗体和疫苗方法均未能中和并保护其免受 CoV 感染。在这些发现的基础上,我们重新合成了一种传染性全长 SHC014 重组病毒,并在体外和体内证明了强大的病毒复制。我们的工作表明,目前在蝙蝠种群中传播的病毒存在重新出现 SARS-CoV 的潜在风险。
主要的SARS-CoV 的出现预示着严重呼吸道疾病跨物种传播的新时代,全球化导致了全球范围内的快速传播和巨大的经济影响3、4。从那时起,动物种群中出现了几种毒株,包括甲型流感毒株 H5N1、H1N1 和 H7N9 以及 MERS-CoV,给受灾地区造成了相当大的疾病、死亡率和经济困难5。尽管公共卫生措施能够阻止 SARS-CoV 的爆发4,但最近的宏基因组学研究已经确定了在中国蝙蝠种群中传播的密切相关的 SARS 样病毒序列,这些病毒可能对未来构成威胁1 , 6. 然而,仅凭序列数据就无法识别和准备未来的大流行前病毒。因此,为了检查循环蝙蝠 CoV 的出现潜力(即感染人类的潜力),我们构建了一种嵌合病毒,该病毒编码一种新型的人畜共患 CoV 刺突蛋白——来自从中国马蹄蝠中分离的 RsSHC014-CoV 序列1 ——在 SARS-CoV 小鼠适应骨干的背景下。杂交病毒使我们能够独立于其天然骨架中其他必要的适应性突变来评估新型刺突蛋白引起疾病的能力。使用这种方法,我们在原代人类呼吸道细胞和体内表征了由 SHC014 刺突蛋白介导的 CoV 感染,并测试了现有免疫疗法对 SHC014-CoV 的功效。该策略共同转化宏基因组学数据,以帮助预测和准备未来出现的病毒。
https://www.nature.com/articles/nm.3985
 https://blog.creaders.net/u/8994/202106/405873.html
|
