纽约时报最近发表了一篇报道,讲了mRNA新冠疫苗的研发历史。看完后又接着看了很多其他相关的报道,觉得这样一个精彩的故事应该让更多的人们了解到,看看科技如何创造了奇迹。下面的文字综合了纽约时报以及其他很多媒体的内容,以飨大家!
序
如果从研发成功的速度以及惠及的人群来说,辉瑞/BioNTech和Modena的mRNA新冠疫苗恐怕是人类历史上最成功的一次了。要知道,从2000年到2020年的整整20年间,美国政府累计投入了超过15亿美元,做了上百次临床试验,都没有能成功研发出艾滋病疫苗来。60年代问世的最快的麻疹疫苗也花了四年的时间。那么,mRNA 新冠疫苗真的是奇迹吗?
一项大的科技突破,需要政府的对于基础科学研究的财政资助,需要不畏艰辛的耐于寂寞的科学家们的长年的大胆探索,需要风险资本的超前投入,以及强有力的知识产权保护和创新机制。
上世纪60年代科学家们初步解开了生命的核心秘密。人们开始认识到基因是如何将二维密码变成三维的无比丰富的蛋白质以及其衍生出来的生命形态。对于基础科学的突破,其带来的巨大收益往往是最初发现者都完全无法想象的。如果将一次次重大突破连成时间轴的话,我们就会发现技术创新速度是在不断加速,而且是跳跃式的。
一
让我们回到起点。自从1800世纪末英国医生爱德华詹纳首次发明了天花疫苗后,人类在与病毒的斗争中开始取得长足的进步。特别是40年代后一系列疫苗(比如百白破,麻腮风、水痘、脊灰等)的推出,年幼儿童死亡率大幅下降。以美国为例,1800到1900这一百年,儿童死亡率从462/千人下降了一半到238/千人,但从1900到2000,儿童死亡率大幅下降到了9/千人。尽管如此,人类在对病毒的了解上仍然处于摸索阶段。瘟疫仍然时常发生。1981年,美国首次报道了全新的病毒-HIV引发的可怕的艾滋病例,其后20年间,艾滋病在全球肆虐,累计感染7000多万,死亡3500多万。全球医药巨头们接连开发了抗病毒药物,大大降低了死亡率。但研发疫苗来预防艾滋病一直是政府、企业和科学家们共同的孜孜以求的目标。
1996年底,美国艾滋病累计死亡病人已达到35万人,全球超过600万人,形势非常严峻。总统克林顿叫来了福奇博士询问为何艾滋病已经过了十几年了还没法研发出疫苗。福奇的回答是因为艾滋病研究布局分散,没有统一协调,所以进展缓慢。克林顿随后决定拨款建立疫苗研究中心。正是这样一个决定,引来了两个关键人物。
Barney Graham博士是新成立的疫苗研究中心首批招募的科学家之一。他从1981年起还在当住院医生时被最初的几起艾滋病例惨状所震惊,随后便立志要成为病毒学家,攻克这个死亡杀手。Graham博士2000年来到疫苗研究中心后,随即带领团队开始了艾滋病疫苗的研发。在研究中,他们发现艾滋病毒主要通过其表面的刺蛋白进入到人体的T细胞。所以如果能开发出针对这个刺蛋白的抗体,那么疫苗就胜利在望了。但随后他们就发现这是个非常难的挑战。原因在于艾滋病毒的刺蛋白形状不断地在变化,如果开发的抗体针对的不是最有效的那个形状,那么疫苗的有效率也就不可能很高。Graham的团队几年下来一直被这个难题所困住。

2008年,29岁的X射线晶体学家Jason McLlellan加入了疫苗研究中心,加大了攻关力度。不过由于艾滋病毒的快速突变,McLlellan干了半年左右就有点厌倦了,感觉找不到突破口。于是,他向老板要求能不能研究点别的病毒。 按说,当时中心招他就是为了攻克艾滋病毒的,现在他撂挑子不想干了,估计大多数老板会很不高兴。幸运的是他当时的老板来了个民主投票,结果大伙同意他另辟蹊径。Graham提议他研究RSV病毒。尽管Graham已经对这个病毒研究了很多年,但还是对病毒表面的蛋白如何与人体细胞融合很困惑。当时的科学家们已经认识到RSV的融合蛋白存在两种状态: 融合前和融合后。两种状态下的蛋白外形完全不同。而当时很多疫苗都把焦点放在了融合后的蛋白结构上,导致病毒中和能力不高。除了这个棘手的难点外,还有一个更让人头疼的问题。那就是融合前的蛋白活脱脱就像个变形金刚,你看他一次,他已变了几次。仿佛在向科学家们示威:哈哈,尔等其奈我何?

有时灵感就在一刹那。Graham和McLlelan 有一天突然想到为什么不想个法子试试把蛋白稳定下来呢?这时,McLlellan的杀手锏使出来了。经过精心的准备,他终于首次通过X射线晶体学实验拍到了蛋白的三维外形。这一发现让Jason如获至宝。他接着想出了绝招,改变了蛋白的局部氨基酸结构,终于使得蛋白稳定了下来。在接下来的动物试验中,他们的新疫苗的抗体滴度大幅上升了50倍。他们的这一技术被评为2013年科学杂志的年度突破性技术!
这就像足球的临门一脚!Jason和Graham的新技术万事俱备,只欠东风。2013年,Jason来到德州大学创办了自己的实验室。问到未来的研究方向,Graham建议冠状病毒。这在当时,冠状病毒还是个不太引人关注的最多引起感冒的东东,政府也没有多大兴趣给予足够的研究赞助。将实验室押注在它上面看上去就是个赌博。不过,Graham却好似冥冥中发现了什么。一是年轻科学家将研究定位在少数人关注的领域可能竞争更少,更容易出成果。二是,2003年爆发的中国非典,以及2012年刚刚爆发的死亡率极高的MERS,让他隐隐担忧冠状病毒的未来再次爆发。碰巧的是,Graham的一个中东同事从麦加朝圣回来似乎感染了MERS。幸运的是他没中招,但感染了另一种冠状病毒:HKU1。好在HKU1病毒的刺蛋白稳定了好多。他们和另一家研究机构合作,通过最先进的冷冻电镜来观察病毒的结构。2016年他们成功地在《自然》杂志上发布了HKU1的融合前刺蛋白的三维图片。2017年的诺贝尔化学奖正是授予三位发明了冷冻电镜技术的科学家。
终于,现在来到了最关键的关口,如何攻克MERS病毒。新的人物登场。来自清华大学的博士后研究人员-王年爽,在看到Jason的RSV研究成果后很激动,2014年申请到Jaosn的实验室工作。之前,他在国内已经对MERS病毒有了较深的研究。到了美国之后,他随即开始了紧张的研究,如何将飘忽不定的MERS的刺蛋白稳定下来。经过几次三番的尝试后,他们惊喜地发现加上两个脯氨酸后,MERS病毒的刺蛋白终于变得温顺了下来。当他们试图将这个突破性的研究结果给五大顶级刊物投稿时,竟然被拒绝了。为何?因为到了2017年,MERS疫情已经结束了,再也没有多少人对其感兴趣。对于王博士来说,这次打击很大,毕竟付出了三年的汗水,因为论文发表的失败使得他无法申请更好的工作。这一切直到2020年1月,一场突如其来的疫情改变了很多人的一切!Graham刚刚拿到中国科研人员的新冠病毒的基因序列,随便立马打电话给McLlellan,问想不想大干一场?回答是:马上干!两个实验室的团队利用之前的成功经验终于开发出了稳定版的新冠刺蛋白。这项关键技术后来被Moderna和辉瑞/BioNTech的疫苗团队采纳。至此,新冠疫苗的三大重大突破之一算是有谱了。
二
花开三朵,各表一枝。自从上世纪60年代基因发现后,引无数英雄竞折腰。我们的主角之一-Katalin Kariko开始登场。1955年出生于匈牙利的Kariko从小就迷上了生物学,而60年代信使RNA的发现更是让她痴迷不已。她似乎看到了mRNA的无限潜力。只不过梦想是美好的,现实是残酷的,到了1985年,她所在的匈牙利大学实验室经费花光了,她不得不考虑未来的前途。她和老公一商量,得,咱还是去美国撞大运吧!于是,两人变卖了所有的家产,带着一千多元美元和小女儿远赴美国。据说当时的匈牙利外汇管制很严,每人只许携带100美元。夫妻俩想了个办法,把多余的美元藏在女儿的书包里,冒着走私外汇的风险,闯过了匈牙利海关。

来到美国后,Kariko过上了美漂生活。尽管是个博士,但其实就是个低价劳动力辗转在各个实验室之间。每当实验室老板不再需要或者没钱时,她就要重新找活。基本上她就是一个三无人员-无永久职位,无政府赞助,无论文发表。按说换成另一个人,可能意味着她的学术生涯从此就了结了,之后沉没在普罗大众中,或者改行去卖药也是个出路。不过,Kariko显然不是一般人。她就像修道者一样追随者自己的激情,天天泡在实验室,一心埋在科研中。由于mRNA众所周知的原因,大多数同行们对于它的医学潜力都非常怀疑。1989年她辗转来到了宾大的一个实验室,继续进行了很多mRNA的研究。但这个过程注定很艰辛,充满了失败。1995年,一度她连职位都被宾大降级了。换成普通人,可能已经放弃了,看不到希望啊!雪上加霜的是,这时她还被诊断出癌症。让人敬佩的是,她毫不气馁。1998年,一个偶然的机会,她在一台复印机旁遇见了正在宾大从事艾滋病疫苗研究的Drew Weissman博士。她毛遂自荐,说她很精通如何从mRNA制成各种蛋白质,甚至包括疫苗。Weissman博士当时也苦于找不到突破,想想何不试试新的mRNA技术。于是Kariko开始和Weissman合作,继续她的mRNA研究。一次,Kariko拿出她的合成mRNA注射到老鼠身上,满怀希望有奇迹发生。遗憾的是,这次试验是个巨大的失败。老鼠身上的毛都掉了,不跑也不进食,还有一些老鼠因此死了。也就是说她的mRNA分子毒性很大。这让Kariko一度觉得绝望,难道真的mRNA不能成药吗?那些一直嘲笑她的人真的看对了?好在两人都没放弃。他们继续不断尝试,尝试找到原因和新的方法。
终于到了2005,苦尽甘来。他们研究发现,他们合成的mRNA被细胞内的免疫系统攻击,并导致免疫反应。但细胞自己的RNA,比如tRNA却不会被攻击。他们通过仔细的分析发现,原来细胞自身的RNA做了一番修改,其中最关键的是假尿嘧啶。于是,他们如法炮制,用假尿嘧啶修改了原来的合成mRNA,结果令他们大喜过望,mRNA成功地在细胞内生成了蛋白质。
正如王年爽一样,他们满怀希望地把他们的突破性科研成果向几大顶尖刊物投稿,都被拒绝了,最后在2005发布在了免疫学杂志。两人还幻想着接下来每天会接到N个电话找他们合作。讽刺的是,没有一个人打来电话。两人感到非常的沮丧。但也不能就此拉倒啊。于是他们注册了一家名叫RNARx的公司,不过到了2013年公司就关闭了。

好在新生事物终究是不可战胜的。事实上两人的科研成果引起了少数企业的高度关注。创立于2010年的新兴生物科技企业Moderna已经盯上了这个新兴的方向。后文再表。
三
mRNA的不稳定以及很快被人体内的酶降解一直是个头号挑战,也是mRNA临床研究进展缓慢的重要原因。如果没有下面这个重大技术的跨越数十年而来的突破,恐怕,这轮新冠疫情会给人类造成更多的病亡!
出生于1946年的加拿大科学家Pieter Cullis 早年是个实验物理学家,如今被视为加拿大生命科学界的教父。他在牛津大学做博士后的时候,有一天突然感到物理学界的重大发现好像都被前人摘走了,他只好希望在别的领域有所建树。最后他将目光落在细胞膜上。人体内的上万亿的细胞表面都有双层脂质膜,将细胞隔成内外两个环境。而神奇的脂质膜还扮演者细胞的众多关键的功能。Cullis想能否开发出类似的膜来将药物分子包装进来,然后再进入细胞。八十年代末,他来到温哥华的UBC,建立了自己的实验室,开始了脂质体技术研发的漫长征程。九十年代,恰逢基因疗法一度成为科研热潮。为了将基因携带到体内,正好需要特殊的载体。
要想开发出大自然花了数千万年才进化出来的类似脂质膜这样的分子结构注定是极为艰辛的。刚开始的几年,费尽心血开发出来的产品遭遇了很多的失败。其中一个大的挑战就是他的脂质膜带有正电荷,会把正常细胞膜击破,因而有很大的毒性。后来,他的团队终于攻克难关,使得脂质体到了人体血液中后就失去极性。尽管如此,还有很多挑战。Cullis开始有点灰心,因为赚不到什么钱。于是他开始转向其他药物研发领域,并将脂质体技术授权给了另一家公司Protiva。2004年,Protiva跨出关键一步:成功将基因材料包装到脂质体中。
正好Kariko他们一直在寻找最好的mRNA的载体技术。看到Protiva的成果后非常激动。随即想说服Protiva的首席科学家过来一起工作。不过由于各种专利纠纷没能成行。直到Kariko后来到了BioNTech后,才与Cullis的后来的新公司Acuitas重新开始了合作。正是Acuitas与Alnylam的长期合作,才开发出了第一款RNA干扰药物Onpattro。2012年后,Cullis想既然LNP可以递送干扰基因,那也可以递送表达基因。此后,他们成功地将mRNA递送到了肝细胞内。2014年,Weissman他们也开始与Cullis合作开发疫苗。
至此,加上Jason和Graham的刺蛋白稳定技术,三大技术准备到位,终于集大成于一体,辉瑞/BioNTech和Moderna才开发出了新冠mRNA疫苗。
四
创立于2010年的Moderna,是最近十年的美国最大生物科技独角兽之一。创始人包括声名显赫的Tim Springer和Rob Langer。据说Langer 博士是史上论文引用次数最多的工程师!另一个发起创始人,加拿大籍的Derrick Rossi,2005年还在哈佛从事博士后干细胞研究的时候,正好看到了Kariko的那篇论文,他受到很大的启发,借用他们的科研成果成功地改变了干细胞的基因。Moderna的含义就是Modified RNA。接下来他们拿到了著名 Flagship 先锋风投基金的投资。不过,在2020年之前,Moderna的研发主要不是在疫苗,而是在其他领域,比如心血管疾病、罕见病、癌症等。但他们已经在疫苗的几个核心技术上有了足够的积累。Moderna公司文化比较神秘,几乎从来不发表什么论文,也不会分享多少临床数据。但公司的CEO是个能人,在上市前融资已经超过10亿美元。Moderna的疫苗之路远远不是表面上看起来那么顺利。公司2018年上市,但到了2019年底,资金已经很紧张了。2020年1月,新冠疫情开始爆发后,公司的几个大的投资机构纷纷表示不愿意公司“分心”到可能血本无归的疫苗研究上,特别是新冠这样一个所知甚少的新病毒。即便疫苗研发出来了,还需要巨额的生产线设备投资。公司CEO Stephane Bancel为资金奔波了数月,甚至还跟多年的合作伙伴默克洽谈过。但默克的传染病部门就和大多数同行一样对mRNA深表怀疑(还指望大公司有颠覆性创新吗?),最后不了了之。新冠疫苗的研发实际上是个残酷的竞赛。如果别人提前研发生产并占领了市场,那么后来者的机会就很低了。当时,辉瑞、阿斯利康、强生都是齐头并进。川普政府也特别推出了光速计划加快疫苗的投资和审批流程。到了5月中旬,公司终于引来转机。一期临床数据揭晓,效果显著,公司股价飙升20%。其后,公司宣布再次融资,尽管仍然有很多怀疑声音,摩根斯坦利还是决定赌一把,承销了十多亿。有了资金,公司迅即开始了规模化量产的投资。后来的故事大家都知道了。新冠疫苗的审批速度创有史以来之最!从零到一的过程惊心动魄,一方面需要非凡的实力,另一方面,也需要特别的运气!十年磨一剑已经算是很幸运的了!
而土耳其移民Ugur Sahin夫妻创业档则在2008年创立了BioNTech,旨在开发当时新兴的针对癌症的个性化免疫疗法。夫妻俩是典型的科研狂。据说在他们举行婚礼的当天,早上两人还去实验室工作,然后参加婚礼,婚礼结束后再次回到实验室工作。

他们早在90年代就开始关注mRNA方面的科研进展,看上去有点离经叛道。2013年他们把Kariko招了起来领衔该领域的研发。不像Moderna,BioNTech则从一开始就发表了很多研究论文。可能这与Sahin本身花很多时间还活跃在学术第一线有关。2019年10月公司在纳斯达克上市。2020年1月当新冠疫情的新闻刚刚报道出来时,Sahin就敏锐地意识到这个病毒可能会在全球蔓延。为此,他说服了所有的内部员工,并且召开了紧急会议,决定迅速展开新冠疫苗的研发。和BioNTech跟Moderna不同的是,他们很快就选定了财大气粗的辉瑞作为合作伙伴,因此不用担心资金的问题。辉瑞的老板和Sahin可以说是一拍即合。之后,双方都是以光速般的速度展开了研发、建厂、生产、测试等流程,在非常不确定的背景下取得了空前的成功!下图可以看到疫苗的正常时间表
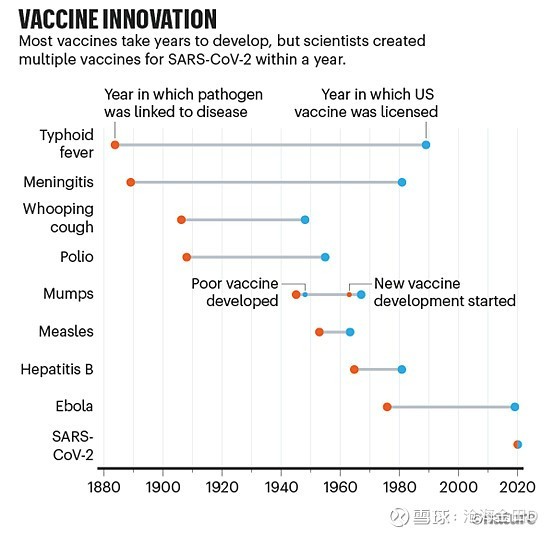
回首往事,这是一个跨越四十年的伟大征程!我们会发现这些重大技术突破的背后都深藏着科学家们征服未知世界的研究激情!无论是Graham,还是Jason,Kariko,和Cullis,都在他们专注的领域数十年如一日地偏执狂一般地投入,很多还饱受冷眼和讽刺。也没有人想到过他们的研究有朝一日能够拯救数百万人的生命!同时,技术的突破是个漫长的进程,需要在多个领域经由无数科研人员的努力,只是在关键的时刻戏剧般地加速了。尽管每个研究人员的课题是随机的,但这些随机的科研活动促成了整个技术层面的向前进化,最终汇成了技术的大海,让后人能够借助前人的智慧不断推进。试想,如果没有冷冻电镜这样的酷科技,我们又如何第一时间得知病毒的结构呢?没有先进的基因测序设备,我们又如何获取并合成病毒的基因呢?而所有这些科技的背后,又离不开政府在基础科学领域的持续投入。
技术的突破往往带有偶然性,因此也是不可预测的。福奇建立疫苗研究中心本来是用来研制艾滋病疫苗的,最后成功的却是新冠疫苗。Graham如果没遇见新冠病毒,可能也早已退休,颐养天年了。如果靠谁来提前规划科技创新的具体路线,往往是事与愿违的。
说到创新药,从mRNA可以看到,大型药企很少是创新的来源。颠覆性技术大多数来自研究机构的标新立异的科学家们的好奇心驱使。而政府的资助经费一般也比较有限,所以发达的风投体系很关键。早期风投的投资家们很多也是有着狂热的技术梦想,他们去投资一些科学狂人,往往最后会溅射出人类重大科技发明的火花。但是要把创新成果最后变成普罗大众能享用的药品,还得需要大大小小的制药企业们。
我们如今能自由生活在奥密克戎依旧肆虐的世界中,谨向这些科学家们致以无比的敬意和谢意!

共存vs清零——与中国流行病学首席专家吴尊友先生的商榷【时政大视野】第54期(音频)